题目内容
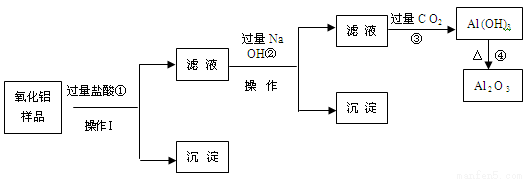
(18分)某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题:
(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为:
、 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。
(1)SiO2 ,Fe(OH)3 (2)Fe+2H+= Fe2++H2↑; Fe+2Fe3+=3 Fe2+;(3)过滤, 引流。
【解析】
试题分析:由分离流程可知,氧化铝样品中含有氧化铁和二氧化硅杂质,加入过量盐酸,氧化铝与过量盐酸反应生成氯化铝,氧化铁和盐酸反应生成氯化铁,二氧化硅不与盐酸反应,则操作I为过滤,得到沉淀A为SiO2,滤液A中含氯化铝、氯化铁、盐酸,再加入过量NaOH,氯化铝与碱反应生成偏铝酸钠和氯化钠,氯化铁与碱反应生成氢氧化铁沉淀和氯化钠,盐酸与碱反应生成氯化钠,则操作为过滤,得到沉淀B为Fe(OH)3,滤液中有NaAlO2、NaCl、NaOH,再通入过量的二氧化碳,与NaAlO2反应生成Al(OH)3,分解生成氧化铝,(1)由上述分析可知,沉淀A为SiO2,沉淀B为Fe(OH)3;(2)滤液A中含氯化铝、氯化铁、盐酸,则滤液A中若加入过量的铁粉,可能发生的所有离子方程式为Fe+2H+= Fe2++H2↑、Fe+2Fe3+=3 Fe2+;(3)由上述分析可知,操作I为过滤,玻璃棒的作用为引流。
考点:考查物质的分离提纯实验方案设计。

练习册系列答案
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
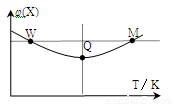
 3Z(g)△H<0反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。
3Z(g)△H<0反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。