题目内容
(每空2分,共10分)某溶液中仅含有下表中的一些离子(不考虑水的电离和离子的水解)
|
阳离子 |
Na+ Mg2+ Fe2+ Al3+ Fe3+ |
|
阴离子 |
OH- Cl- CO32- NO3- SO42- |
为鉴定这些离子,取少量溶液加入稀HCl,有无色气体生成。该气体遇空气变为红棕色,且溶液中阴离子的种类不变;
(1)通过分析该实验,能确定溶液中一定存在的阳离子是 。一定存在的阴离子是 。
(2)写出实验中发生的离子方程式 。[来源:Z,xx,k.Com]
(3)通过对实验的分析,尚不能确定溶液中是否存在的阴离子是 ,如何进一步鉴别该离子是否存在 。
(每空2分,共10分)(1)(1) Fe2+ Cl- 和NO3-
(2) 3Fe2+ + 4H+ + NO3- ==3Fe3+ + 2H2O + NO↑
(3) SO42- 取少量原溶液,加入盐酸酸化BaCl2溶液,若产生白色沉淀,则证明有SO42-;
【解析】加入稀HCl,有无色气体生成。该气体遇空气变为红棕色,所以气体是NO,则说明加入盐酸后NO3-发生了氧化还原反应,因此一定含有亚铁离子,则就不能含有OH-和CO32-。由于溶液中阴离子的种类不变,所以一定含有氯离子,而SO42-不能确定。要确定SO42-则可以利用盐酸酸化的氯化钡进行检验,即取少量原溶液,加入盐酸酸化BaCl2溶液,若产生白色沉淀,则证明有SO42-。

(每空2分,共10分)食品安全关系国计民生,影响食品安全的因素很多。
(1)聚偏二氯乙烯(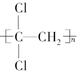 )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
(2)劣质植物油中的亚油酸[CH3(CH2)4—CH===CH—CH2—CH===CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是________。
| A.分子式为C18H34O2 |
| B.一定条件下能与乙酸发生酯化反应 |
| C.能和NaOH溶液反应 |
| D.能使酸性KMnO4溶液褪色 |
(4)劣质奶粉中蛋白质含量很低。蛋白质水解的最终产物是__________________。
(5)在淀粉中加入吊白块制得的粉丝有毒。淀粉最终的水解产物是葡萄糖。请设计实验证明淀粉已经全部水解,写出操作、现象和结论:_________________________________。
 )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。