题目内容
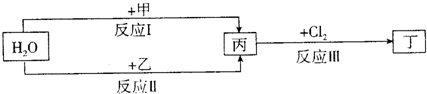
有A、B两种常见化合物,其焰色反应均呈现黄色,相互转化关系如下图(其他物质均已略去)。
(1)化学式:A ;B ;C 。?
(2)B加热产生D的化学方程式: ;B加稀硫酸产生D的离子方程式: 。?
(3)A、B加热后,若只得一种固体化合物,则A与B的物质的量之比的最大值为? (填数字)。
(1)Na2O2 NaHCO3 O2?
(2)2NaHCO3![]() Na2CO3+CO2↑+H2O?
Na2CO3+CO2↑+H2O?
H++HCO![]()
![]() H2O+CO2↑?
H2O+CO2↑?
(3)![]()
解析:本题考查的是有关钠的化合物Na2O2、NaHCO3、NaOH的有关化学性质,Na2O2与H2O反应可生成NaOH和O2,NaHCO3与稀H2SO4可放出CO2,NaOH与过量的CO2反应又可生成NaHCO3。Na2O2和NaHCO3加热后,若只得Na2CO3,根据Na、C守恒可得Na2O2、NaHCO3物质的量之比最大值为1∶2。

现有A、B、C、D四种短周期非金属元素,它们的原子最外层电子数之和为19。在它们的化合物中,主要化合价均不止一种,但都有一种相同的化合价,C的单质常用于太阳能电池。它们的一些物理量如下:
| 元素 | A | B | C | D |
| 原子半径/nm | 0.102 | 0.077 | 0.117 | 0.075 |
| 单质的沸点/℃ | 444.6 | 4827 | 2355 | –195.8 |
(1)A的元素符号为__________,D元素在周期表第_______周期、第_______族。
(2)在常温下,B与C的最高价氧化物分别为气态和固态,原因是____________________。
(3)含D的两种常见化合物发生化合反应可生成一种离子化合物,该离子化合物撞击时可分解为两种非金属单质和一种化合物,其中一种为D单质,写出该分解反应的化学方程式____________________________________________________________________。
(4)A、B、C、D均能分别形成含18个电子的氢化物,这些氢化物的分子式分别是________________________________________________。
(5)B、D及氢元素中的两种或三种可形成多种含14个电子的化合物,其中空间构型为直线型的是_______________________和_______________________(写结构式)。
 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.