题目内容
 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是
S2->O2->Na+
S2->O2->Na+
(填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于离子键、共价键
离子键、共价键
.(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为:
2Al+2OH-+2H2O=2AlOH2-+3H2↑
2Al+2OH-+2H2O=2AlOH2-+3H2↑
.(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为
H2+CO32--2e-=CO2↑+H2O
H2+CO32--2e-=CO2↑+H2O
.用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时,NaCl溶液的PH=13
13
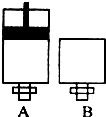
(假设电解过程中溶液的体积不变)(4)可逆反应2EC2(气)+C2(气)?2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B 容器可保持恒容 (如图所示),若在 A、B 中分别充入lmolC2 和2molEC2,使V(A )=V( B ),在相同温度下反应,则:①达平衡所需时间:t(A )
<
<
t( B )(填>、<、二,或:无法确定,下同).平衡时 EC2 的转化率:a( A )>
>
a( B ).(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有
cd
cd
(填“序号”).a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易.
分析:A、B、C、D、E为原子序数依次增大的五种短周期元素,B、C、E在周期表中相邻,且C、E同主族,原子序数C大于A、B小于E,则C处于第二周期,E处于第三周期,所以B、C、E在周期表中的位置关系为 ,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,据此解答.
,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,据此解答.
 ,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,据此解答.
,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,据此解答.解答:解:A、B、C、D、E为原子序数依次增大的五种短周期元素,B、C、E在周期表中相邻,且C、E同主族,原子序数C大于A、B小于E,则C处于第二周期,E处于第三周期,所以B、C、E在周期表中的位置关系为 ,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,
,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,
(1)电子层结构相同核电荷数越大离子半径越小,最外层电子数相同电子层越多离子半径越大,故离子半径S2->O2->Na+;
由H、N、O三种元素按 4:2:3组成的化合物为NH4NO3,含有离子键、共价键,
故答案为:S2->O2->Na+;离子键、共价键;
(2)H、O、Na组成的化合物为NaOH,废弃的金属易拉罐含有Al,铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlOH2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlOH2-+3H2↑;
(3)氢气、氧气与熔融K2CO3,组成的燃料电池,氢气在负极放电,在熔融碳酸钾条件下生成二氧化碳与水,电解反应式为:H2+CO32--2e-=CO2↑+H2O;
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LH2时,氢气的物质的量=
=0.05mol,生成的NaOH物质的量=0.05mol×2=0.1mol,故n(OH-)=0.1mol/L,则c(H+)=
=10-13,故l溶液的pH=-lg10-13=13,
故答案为:H2+CO32--2e-=CO2↑+H2O;13;
(4)可逆反应2EC2(气)+C2(气)?2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B 容器可保持恒容 (如图所示),若在 A、B 中分别充入lmolC2 和2molEC2,使V(A )=V( B ),在相同温度下反应,则:A中压强不变,B中压强减小,故A反应速率更快,达平衡所需时间更短,故t(A)<t(B);A中的压强更高,增大压强平衡向正反应反应移动,平衡时 EC2 的转化率更高,故:a( A )>a( B ),
故答案为:<;>;
(5)a.沸点属于物理性质,不能比较元素的非金属性强弱,故a错误;
b.单质的状态属于物理性质,不能比较元素的非金属性强弱,故b错误;
c.气态氢化物的稳定性,元素的非金属性越强,可以利用氢化物稳定性比较,故c正确;
d.元素的单质与氢气化合的越容易,单质越活泼,元素的非金属性越强,故d正确;
故答案为:cd.
 ,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,
,A和D最外层电子数相同,则二者处于同族,原子序数D大于C小于E,则D为第三周期,其中仅含一种金属元素,D应为金属,B、C的最外层电子数之和等于D的原子核外电子数,D的核外电子数为奇数,则D为钠元素或铝元素,若D为钠元素,则A为氢元素,B为氮元素,C为氧元素,E为硫元素,A和C可形成化合物H2O、H2O2,二者是常见的液态化合物,符合题意.若D为铝元素,则A为硼元素,B为氧元素,C为氟元素,E为氯元素,A和C形成化合物,不符合题意.故A为氢元素,B为氮元素,C为氧元素,D为钠元素,E为硫元素,(1)电子层结构相同核电荷数越大离子半径越小,最外层电子数相同电子层越多离子半径越大,故离子半径S2->O2->Na+;
由H、N、O三种元素按 4:2:3组成的化合物为NH4NO3,含有离子键、共价键,
故答案为:S2->O2->Na+;离子键、共价键;
(2)H、O、Na组成的化合物为NaOH,废弃的金属易拉罐含有Al,铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlOH2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlOH2-+3H2↑;
(3)氢气、氧气与熔融K2CO3,组成的燃料电池,氢气在负极放电,在熔融碳酸钾条件下生成二氧化碳与水,电解反应式为:H2+CO32--2e-=CO2↑+H2O;
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LH2时,氢气的物质的量=
| 1.12L |
| 22.4L/mol |
| 10-14 |
| 0.1 |
故答案为:H2+CO32--2e-=CO2↑+H2O;13;
(4)可逆反应2EC2(气)+C2(气)?2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B 容器可保持恒容 (如图所示),若在 A、B 中分别充入lmolC2 和2molEC2,使V(A )=V( B ),在相同温度下反应,则:A中压强不变,B中压强减小,故A反应速率更快,达平衡所需时间更短,故t(A)<t(B);A中的压强更高,增大压强平衡向正反应反应移动,平衡时 EC2 的转化率更高,故:a( A )>a( B ),
故答案为:<;>;
(5)a.沸点属于物理性质,不能比较元素的非金属性强弱,故a错误;
b.单质的状态属于物理性质,不能比较元素的非金属性强弱,故b错误;
c.气态氢化物的稳定性,元素的非金属性越强,可以利用氢化物稳定性比较,故c正确;
d.元素的单质与氢气化合的越容易,单质越活泼,元素的非金属性越强,故d正确;
故答案为:cd.
点评:本题考查结构与位置关系、半径比较、晶体类型与化学键、原电池、化学计算、化学平衡移动、非金属性比较等,难度中等,是对知识综合运用与学生能力考查,推断元素是关键,需充分利用信息,对知识全面掌握,物质推断是难点、易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【化学--选修3:物质结构与性质】
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)G位于 族 区,价电子排布式为 .
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈
形.
(3)画出C原子的电子排布图 .
(4)已知BA5为离子化合物,写出其电子式 .
(5)DE3中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型为 .
(6)用电子式表示F元素与E元素形成化合物的形成过程 .
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
形.
(3)画出C原子的电子排布图
(4)已知BA5为离子化合物,写出其电子式
(5)DE3中心原子的杂化方式为
(6)用电子式表示F元素与E元素形成化合物的形成过程
 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:

