题目内容
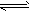 FeO(s)+CO(g) △H1=a kJ/mol;②CO(g)+1/2O2(g)
FeO(s)+CO(g) △H1=a kJ/mol;②CO(g)+1/2O2(g)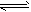 CO2(g) △H2=b kJ/mol 测得在不同温度下,反应①的平衡常数K值随温度的变化如下
CO2(g) △H2=b kJ/mol 测得在不同温度下,反应①的平衡常数K值随温度的变化如下
(2)700℃反应①达到平衡,要使该平衡向右移动,其他条件不变时,可以采取的措施有____(填序号)。
A.缩小反应器体积 B.通入CO2 C.升高温度到900℃ D.使用合适的催化剂
(3)下列图象符合反应①的是____(填序号)(图中v是速率、
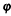 为混合物中CO含量,T为温度且T1> T2)
为混合物中CO含量,T为温度且T1> T2) 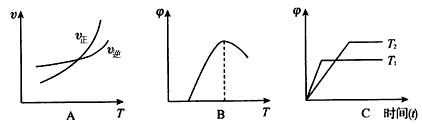
 2FeO(s) △H3,该反应的△H3=____kJ/mol。
2FeO(s) △H3,该反应的△H3=____kJ/mol。 (2)BC
(3)A
(4)2(a+b)

(10分)设反应①Fe(s)+CO2(g)FeO(s)+CO(g) △H = Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+H2(g) △H = Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
| 温度( T ) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g)CO(g)+H2O(g) △H = Q
①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂
D.设法减少CO的量 E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3 =_____________;
(12分)下列三个反应在某密闭容器中进行:
反应① Fe(s)+CO2(g) FeO(s)+CO(g) △H1=" a" kJ·mol-1
FeO(s)+CO(g) △H1=" a" kJ·mol-1
反应② 2CO(g)+O2(g) 2CO2(g) △H2=" b" kJ·mol-1
2CO2(g) △H2=" b" kJ·mol-1
反应③ 2Fe(s)+O2(g) 2FeO(s) △H3
2FeO(s) △H3
(1)则△H3= (用含a、b的代数式表示)
(2)已知500℃时反应①的平衡常数K=1.0,在此温度下2L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则
a 0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其它条件不变时,可以采取的措施有 (填序号)。
| A.缩小反应器体积 | B.再通入CO2 |
| C.升高温度 | D.使用合适的催化剂 |
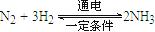 。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。(5)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显___________性(填“酸”“碱”或“中”), 可推断a 0.01(填大于、等于或小于)。
(10分)设反应①Fe(s)+CO2(g) FeO(s)+CO(g) △H = Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) △H = Q1的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g) △H = Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) △H = Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
|
温度( T ) |
K1 |
K2 |
|
973 |
1.47 |
2.38 |
|
1173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g) △H = Q
CO(g)+H2O(g) △H = Q
①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂
D.设法减少CO的量 E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3 =_____________;
(10分)设反应①Fe(s)+CO2(g)  FeO(s)+CO(g)的平衡常数为K1。
FeO(s)+CO(g)的平衡常数为K1。
反应②Fe(s)+H2O(g)  FeO(s)+H2(g)的平衡常数为K2,在不同温度下, K1、K2的值如下:
FeO(s)+H2(g)的平衡常数为K2,在不同温度下, K1、K2的值如下:
|
T(K) |
K1 |
K2 |
|
973 |
1.47 |
2.36 |
|
1173 |
2.15 |
1.67 |
(1)平衡常数K1的表达式为 ________________ 。
(2)现有反应③ CO2(g) +H2(g)  CO(g) +H2O(g);△H>0,这是一个 (填“吸”或“放”) 热反应,要使反应③在一定条件下建立的平衡向右移动,可采取的措施的有
。
CO(g) +H2O(g);△H>0,这是一个 (填“吸”或“放”) 热反应,要使反应③在一定条件下建立的平衡向右移动,可采取的措施的有
。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少CO的量
(3)若反应Fe(s)+CO2(g)  FeO(s)+CO(g)在温度T1下进行;Fe(s)+H2O(g)
FeO(s)+CO(g)在温度T1下进行;Fe(s)+H2O(g)
 FeO(s)+H2(g)在温度T2下进行,已知T1>T2,且c(CO2)>c(CO)(其他条件均相同),则两者的反应速率
(填序号)。
FeO(s)+H2(g)在温度T2下进行,已知T1>T2,且c(CO2)>c(CO)(其他条件均相同),则两者的反应速率
(填序号)。
A.前者大 B.后者大 C.一样大 D.无法判断
(4)以下图像:(图中v为速率,φ为生成物的百分含量,T为温度)

其中符合反应①的是 _________ (填图像序号,下同),符合反应②的是 ___ 。
 FeO(s)+CO(g) △H1,平衡常数为K1
FeO(s)+CO(g) △H1,平衡常数为K1
 增大的是 (填序号)
增大的是 (填序号)