题目内容
铝、溴水、碘酒、干冰、稀硫酸、氯化银固体、氯化氢气体、硝酸钠晶体、淀粉溶液.
上述物质中属于纯净物的是 .
混合物的是 .
属于单质的是 .
属于化合物的是 .
属于离子化合物的是 .
属于共价化合物的是 .
能导电的是 .
属于电解质的是 .
属于非电解质的是 .
上述物质中属于纯净物的是
混合物的是
属于单质的是
属于化合物的是
属于离子化合物的是
属于共价化合物的是
能导电的是
属于电解质的是
属于非电解质的是
考点:混合物和纯净物,单质和化合物,离子化合物的结构特征与性质,共价键的形成及共价键的主要类型,电解质与非电解质
专题:物质的分类专题
分析:只有一种物质组成的是纯净物,由多种物质组成的是混合物;
电解质与非电解质均是化合物,电解质溶于水或熔化状态能导电,非电解质不能导电;
由离子键构成的化合物属于离子化合物,仅由共价键构成的化合物属于共价化合物;
存在自由移动的电子或离子就能导电,依据以上概念分析解答即可.
电解质与非电解质均是化合物,电解质溶于水或熔化状态能导电,非电解质不能导电;
由离子键构成的化合物属于离子化合物,仅由共价键构成的化合物属于共价化合物;
存在自由移动的电子或离子就能导电,依据以上概念分析解答即可.
解答:
解:铝能导电,属于金属单质,既不是电解质也不是非电解质;
溴水能导电,属于混合物;
碘酒能导电,属于混合物;
干冰不能导电,是化合物,非电解质;
稀硫酸能导电,属于混合物;
氯化银固体不能导电,熔化状态下导电,是电解质;
氯化氢气体不能导电,溶于水能导电,属于电解质;
硝酸钠晶体不能导电,溶于水或熔化下能导电,是电解质;
淀粉溶液,属于混合物,
故答案为:
纯净物:铝、干冰、氯化银固体、氯化氢气体、硝酸钠晶体;
混合物:溴水、碘酒、稀硫酸、淀粉溶液;
单质:铝;
化合物:干冰、氯化银、氯化氢、硝酸钠;
离子化合物:氯化银、硝酸钠;
共价化合物:干冰、氯化氢;
能导电:铝、溴水、碘酒、稀硫酸、淀粉溶液;
电解质:氯化银、氯化氢、硝酸钠;
非电解质:干冰.
溴水能导电,属于混合物;
碘酒能导电,属于混合物;
干冰不能导电,是化合物,非电解质;
稀硫酸能导电,属于混合物;
氯化银固体不能导电,熔化状态下导电,是电解质;
氯化氢气体不能导电,溶于水能导电,属于电解质;
硝酸钠晶体不能导电,溶于水或熔化下能导电,是电解质;
淀粉溶液,属于混合物,
故答案为:
纯净物:铝、干冰、氯化银固体、氯化氢气体、硝酸钠晶体;
混合物:溴水、碘酒、稀硫酸、淀粉溶液;
单质:铝;
化合物:干冰、氯化银、氯化氢、硝酸钠;
离子化合物:氯化银、硝酸钠;
共价化合物:干冰、氯化氢;
能导电:铝、溴水、碘酒、稀硫酸、淀粉溶液;
电解质:氯化银、氯化氢、硝酸钠;
非电解质:干冰.
点评:本题主要考查了电解质与非电解质的概念、单质与化合物混合物的感念、粒子的导电性,题目难度不大,注意电解质和导电性的关系,导电的不一定是电解质,电解质不是任何条件下都导电.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
Cl2O与OF2互为等电子体,均能与水反应(与水解反应原理类似),Cl2O与水反应的化学方程式为:Cl2O+H2O=2HClO.下列说法正确的是( )
| A、Cl2O与水的反应属于氧化还原反应 |
| B、OF2、Cl2O分子的立体构型均为直线形 |
| C、Cl2O分子中的共用电子对偏向Cl,OF2分子中的共用电子对偏向F |
| D、OF2与水反应的化学方程式为:OF2+H2O=2HF+O2 |
下列有关化学用语表示正确的是( )
A、CH4分子的球棍模型: | ||
B、Cl-离子的结构示意图: | ||
C、氟化钠的电子式: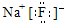 | ||
D、中子数为146、质子数为92 的铀原子
|
人体血液的正常pH约为7.35~7.45,若在外界因素作用下突然发生改变就会引起“酸中毒”或“碱中毒”,甚至有生命危险.由于人体体液的缓冲系统中存在如下平衡:H++HCO3-?H2CO3?CO2+H2O,H++PO43-?HPO42-,H++HPO42-?H2PO4-故能维持血液pH的相对稳定,以保证正常生理活动.下列说法中不合理的是( )
| A、当强酸性物质进入人体的体液后,上述缓冲系统的平衡向右移,从而维持pH稳定 |
| B、某病人静脉滴注生理盐水后,血液被稀释,会导致c(H+)显著减小,pH显著增大,可能会引起碱中毒 |
| C、当强碱性物质进入人体的体液后,上述缓冲系统的平衡向左移,从而维持pH稳定 |
| D、在人体进行呼吸活动时,如CO2进入血液,会使平衡向左移动,c(H+)增大,pH略减小 |
下列物质在水中能分层且下层是水层的是( )
| A、溴苯 | B、苯 | C、四氯化碳 | D、乙酸 |
