题目内容
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA |
| B、标准状况下,0.56 L丙烷中含有共价键的数目为0.25NA |
| C、25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| D、标准状况下,22.4LNH3溶于1L水中得到1.0mol/L氨水 |
考点:阿伏加德罗常数
专题:
分析:A、氯气与水的反应是可逆反应;
B、1mol丙烷中含10mol共价键;
C、Na2CO3的水解程度不明确;
D、氨气溶于水后,溶液的体积不等同于溶剂的体积.
B、1mol丙烷中含10mol共价键;
C、Na2CO3的水解程度不明确;
D、氨气溶于水后,溶液的体积不等同于溶剂的体积.
解答:
解:A、氯气与水的反应是可逆反应,不能进行彻底,故0.1mol氯气转移的电子数小于0.1mol,故A错误;
B、0.56L丙烷的物质的量n=
=
=0.025mol,由于1mol丙烷中含10mol共价键,故0.025mol丙烷中含0.25mol共价键,故B正确;
C、Na2CO3的水解程度不明确,故无法计算pH=12Na2CO3溶液的浓度,故含有的钠离子的个数无法计算,故C错误;
D、氨气溶于水后,溶液的体积不等同于溶剂的体积,故溶液的体积不是1L,则氨水的浓度不是1mol/L,故D错误.
故选B.
B、0.56L丙烷的物质的量n=
| V |
| Vm |
| 0.56L |
| 22.4L/mol |
C、Na2CO3的水解程度不明确,故无法计算pH=12Na2CO3溶液的浓度,故含有的钠离子的个数无法计算,故C错误;
D、氨气溶于水后,溶液的体积不等同于溶剂的体积,故溶液的体积不是1L,则氨水的浓度不是1mol/L,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
0.25mol A的质量是16g,则A的相对分子质量是( )
| A、32 g/mol |
| B、64 g/mol |
| C、32 |
| D、64 |
下列说法中正确的是( )
| A、22.4LO2中一定含有6.02×1023个氧分子 |
| B、将80gNaOH固体溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L |
| C、18gH2O在标准状况下的体积是22.4L |
| D、在标准状况时,20mLNH3与60mLO2所含的分子数之比为1:3 |
下列各组物质的分类正确的是:( )
①混合物:水玻璃、水银、水煤气
②电解质:明矾、醋酸、石膏
③酸性氧化物:CO2、CO、SO3
④同位素:1H、2H2、3H
⑤同素异形体:C80、金刚石、石墨
⑥干冰、液氯都是非电解质.
①混合物:水玻璃、水银、水煤气
②电解质:明矾、醋酸、石膏
③酸性氧化物:CO2、CO、SO3
④同位素:1H、2H2、3H
⑤同素异形体:C80、金刚石、石墨
⑥干冰、液氯都是非电解质.
| A、①②③④⑤⑥ | B、②④⑤⑥ |
| C、②⑤⑥ | D、②⑤ |
某反应过程中的能量变化如图所示.下列说法中正确的是( )


| A、该反应的活化能为E2 |
| B、该反应的△H=E2-E1 |
| C、由图可知,该反应为吸热反应 |
| D、曲线b相对曲线a,改变的条件可能是使用了催化剂 |
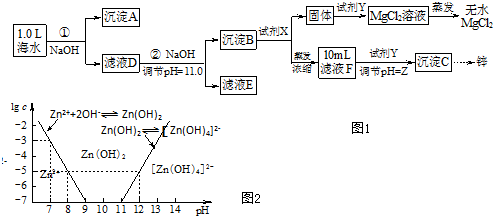

 在图所示的物质相互转化关系中,A是一种固体单质,E是一种白色的溶解度很小的物质.据此填空
在图所示的物质相互转化关系中,A是一种固体单质,E是一种白色的溶解度很小的物质.据此填空