题目内容
信息:

有两种化合物,A:COCl3?5NH3?H2O;B:COCl3?5NH3?H2O,根据下面的实验结果,确定它们的络离子、中心离子和配体。
⑴分别取A和B的固体于试管中微热,A中未见明显现象,B中试管口出现少量水珠。
⑵向A和B的溶液中加入AgNO3溶液后均有AgCl沉淀。
⑶沉淀过滤后,分别向滤液中加AgNO3溶液均无变化,但加热煮沸,B溶液中又有AgCl沉淀生成,其沉淀量为原来B溶液中AgCl的一半。
又已知该化合物中心离子配位数均为6,试按照“[Ag(NH3)2] OH”的书写格式写出A、B的化学式:
A ____________,B ______________。
A:[CO(NH3)5H2O]Cl3;B:[CO(NH3)5Cl] Cl 2?H2O,

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


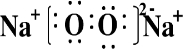
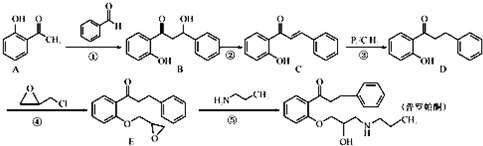
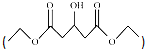 是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用)
是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用)
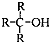 )不能氧化成醛或酮.
)不能氧化成醛或酮.