��Ŀ����
| |||||||||||||||||||
�𰸣�3��������Է�������������е�������;
������
������
(1) |
aΪ,�����ɫ,ɫҺ��;b�ķ���ʽ�ǣ�H2Se |
(2) |
����������;Cl2��2Br����Br2��2Cl��;(�ξ�һ��,�����ӷ���ʽ��ʾ) |
(4) |
HF,H2O���Ӽ����γ���� |

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
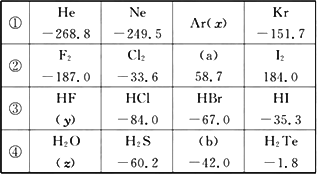
�Т٢ڢۢ��ĸ�ϵ�о�Ϊͬ��Ԫ�ص����ʣ�101.3kPaʱ�ⶨ���ǵķе㣨�棩�����
��Ӧ�������ݣ�������������ȷ���ǣ�������
| �� | He-268.8 | ��a��-249.5 | Ar-185.8 | Kr-151.7 |
| �� | F2 -187.0 | Cl2 -33.6 | ��b�� 58.7 | I2 184.0 |
| �� | ��c�� 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| �� | H2O 100.0 | H2S-60.0 | ��d��-42.0 | H2Te-1.8 |
| A��ϵ�Т����������ʵķе�������������Ϊ���Ӽ�Ļ�ѧ����ǿ |
| B��ϵ�Т����ʾ��������ԣ�ϵ�Т����ʶ�Ӧˮ��Һ����ǿ�� |
| C��ϵ�Т��и���������ȶ���˳��Ϊ��H2O��H2S��H2Se��H2Te |
| D���ϱ������ʣ�c����H2O����е���ͬϵ������������ڷ����ڴ������ |

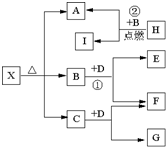 ����A��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ�ص�ԭ���ǰ뾶��С��ԭ�ӣ�BԪ�ص�����������ˮ���������⻯�ﷴӦ����һ����X��D��Aͬ�壬����Eͬ���ڣ�EԪ�ص������������Ǵ�����������
����A��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ�ص�ԭ���ǰ뾶��С��ԭ�ӣ�BԪ�ص�����������ˮ���������⻯�ﷴӦ����һ����X��D��Aͬ�壬����Eͬ���ڣ�EԪ�ص������������Ǵ����������� NH3?H2O+H+
NH3?H2O+H+ ��A��B��C��D����Ԫ�������ڱ��зֱ���Ԫ��X�����ܣ���ͼ������֪XԪ�����������Ļ�ѧʽΪX2O5��������Ԫ������һ��Ԫ�ص�ԭ�Ӱ뾶������������ͬ������С�ģ���ȷ����
��A��B��C��D����Ԫ�������ڱ��зֱ���Ԫ��X�����ܣ���ͼ������֪XԪ�����������Ļ�ѧʽΪX2O5��������Ԫ������һ��Ԫ�ص�ԭ�Ӱ뾶������������ͬ������С�ģ���ȷ����