题目内容
今有甲、乙、丙三瓶等体积的新制氯水,浓度相等.如果在甲瓶中加入少量的NaHCO3晶体,在乙瓶中加入少量的NaHSO3晶体,且两瓶中加入晶体的物质的量相同,丙瓶不变.片刻后,甲、乙、丙三瓶溶液中HClO的物质的量浓度的大小关系是________.(溶液体积变化忽略不计)
答案:
解析:
提示:
解析:
|
甲>丙>乙 因氯水中存在下列平衡: Cl2+H2O |
提示:
|
氯水是混合物,用氯水作试剂发生反应时,一定要理顺的是氟水中什么成分去发生作用,什么成分没有发生反应.一般而言,氯水作氧化剂使用时是Cl2和HClO,且氧化性HClO>Cl2;象氯水的漂白、消毒作用是HClO的强氧化性的体现,象该例中能氧化KHSO3的可以是Cl2也可以是HClO,但HClO应无条件被消耗. |

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
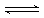 HCl+HClO,加入NaHCO3时,因酸性:HCl>H2CO3>HClO,所以NaHCO3只能和HCl反应而不与HClO反应,平衡向右移动,HClO浓度增大.又因HClO具有强氧化性可将NaHSO3氧化,导致HClO浓度降低.
HCl+HClO,加入NaHCO3时,因酸性:HCl>H2CO3>HClO,所以NaHCO3只能和HCl反应而不与HClO反应,平衡向右移动,HClO浓度增大.又因HClO具有强氧化性可将NaHSO3氧化,导致HClO浓度降低.