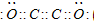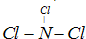题目内容
现有A、B、C、D、E五种原子序数依次增大的短周期元素。已知:A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的邻族元素;D和E的原子序数之和为30;它们两两形成的化合物有甲、乙、丙、丁四种,这四种化合物中原子个数比如下表:
| 甲 | 乙 | 丙 | 丁 |
化合物中各元 素原子个数比 | A∶C=1∶1 | B∶A=1∶2 | D∶E=1∶3 | B∶E=1∶4 |
回答下列问题:?
(1)B元素在周期表中的位置为 。?
(2)丁分子的空间构型为 。?
(3)甲分子的电子式为 。?
(4)已知,乙分子中所有原子共平面,则实验室制取乙的化学方程式为 。
(5)丙的水溶液加热蒸干再灼烧,最后所得固体的成分是(写化学式) 。
(1)第2周期ⅣA族(或第二周期ⅣA族)?
(2)正四面体(写四面体不对)?
(3) ![]() ?
?
![]() ?
?
(5)Al2O3?
解析:短周期元素A、B、C、D、E原子序数依次增大,据B原子最外层电子数比次外层多2个可推知B为碳,据A与B的关系,已知B为碳可推出A只能为氢,C为碳之后的元素与E邻族但原子序数不相邻,故C在第2周期,E在第3周期,D与E原子序数之和为30,且均为短周期,故D也在第3周期,B与E可形成1∶4化合物,故E为Cl,D则为Al,C与E邻族,且与A即H形成1∶1化合物,则C为氧,因此A为H,B为C,C为Al,D为O,E为Cl。

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
 现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.