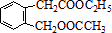题目内容
图中a、b、c、d、e、f表示元素周期表中部分短周期元素,下列叙述正确的是( )

| A.a、b、c的简单离子中,c的离子半径最大 |
| B.c、d、f最高价氧化物对应的水化物两两之间均可发生反应 |
| C.e的氢化物比f的氢化物的稳定性高 |
| D.a、e可形成一种新型无机非金属材料--高温结构陶瓷 |

a、b、c、d、e、f是短周期元素,由各元素在元素周期表中位置可知,a为氮元素、b为氧元素、c钠元素、d为铝元素、e为硅元素、f为氯元素.
A、a为氮元素、b为氧元素、c钠元素,原子形成的离子电子层结构相同,电子层结构相同,核电荷数越大离子半径越小,所以a、b、c的简单离子中,c的离子半径最小,故A错误;
B、c钠元素、d为铝元素、f为氯元素,最高价氧化物对应的水化物为氢氧化钠、氢氧化铝、高氯酸,氢氧化铝是两性氢氧化物,溶于氢氧化钠、高氯酸溶液,氢氧化钠与高氯酸发生中和反应,故B正确;
C、e为硅元素、f为氯元素,非金属性Si<Cl,非金属性越强,氢化物越稳定,所以f的氢化物的稳定性高,故C错误;
D、a为氮元素、e为硅元素,氮化硅是一种新型无机非金属材料--高温结构陶瓷,故D正确.
故选BD.
A、a为氮元素、b为氧元素、c钠元素,原子形成的离子电子层结构相同,电子层结构相同,核电荷数越大离子半径越小,所以a、b、c的简单离子中,c的离子半径最小,故A错误;
B、c钠元素、d为铝元素、f为氯元素,最高价氧化物对应的水化物为氢氧化钠、氢氧化铝、高氯酸,氢氧化铝是两性氢氧化物,溶于氢氧化钠、高氯酸溶液,氢氧化钠与高氯酸发生中和反应,故B正确;
C、e为硅元素、f为氯元素,非金属性Si<Cl,非金属性越强,氢化物越稳定,所以f的氢化物的稳定性高,故C错误;
D、a为氮元素、e为硅元素,氮化硅是一种新型无机非金属材料--高温结构陶瓷,故D正确.
故选BD.

练习册系列答案
相关题目

 +2NaOH
+2NaOH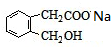 +CH3COONa+CH3CH2OH
+CH3COONa+CH3CH2OH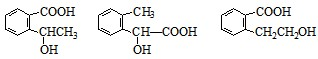 中任意一种
中任意一种 (或CH2=CH2+H2O
(或CH2=CH2+H2O 根据上图回答问题:
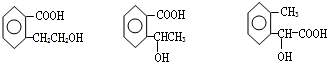
根据上图回答问题: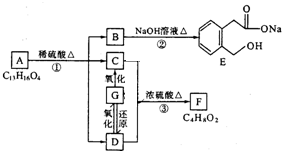 图中A、B、C、D、E、F、G均为有机物,其中B分子内只有一个环状结构.根据图示回答问题:
图中A、B、C、D、E、F、G均为有机物,其中B分子内只有一个环状结构.根据图示回答问题: