题目内容
某有机物的蒸气,完全燃烧时消耗的氧气体积和生成的二氧化碳体积都是它本身体积的2倍.该有机物可能是( )
| A、C2H4 |
| B、H2C═C═O(乙烯酮) |
| C、CH3CHO |
| D、CH3COOH |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:有机物蒸气完全燃烧,产生二倍于其体积的二氧化碳,则分子中含有2个C原子;
对于烃CxHy,耗氧量取决于(x+
),对于烃含氧衍生物CxHyOz,耗氧量取决于(x+
-
),有机物蒸气完全燃烧时需2倍于其体积的氧气,则(x+
)或(x+
-
)的值等于2,结合各选项中分子式,由碳原子及耗氧量进行判断.
对于烃CxHy,耗氧量取决于(x+
| y |
| 4 |
| y |
| 4 |
| z |
| 2 |
| y |
| 4 |
| y |
| 4 |
| z |
| 2 |
解答:
解:令烃CxHy,烃含氧衍生物CxHyOz,
由分析可知,有机物满足分子中含有2个C原子(x+
)或(x+
-
)的值等于2,
A、C2H4分子含有2个碳原子,其(x+
)=2+1=3,故A错误;
B、H2C═C═O分子含有2个碳原子(x+
-
)=2+0.5-0.5=2,故B正确;
C、CH3CHO分子含有2个碳原子,(x+
-
)=2+1-0.5=2.5,故C错误;
D、CH3COOH分子含有2个碳原子(x+
-
)=2+1-1=2,故D正确;
故选BD.
由分析可知,有机物满足分子中含有2个C原子(x+
| y |
| 4 |
| y |
| 4 |
| z |
| 2 |
A、C2H4分子含有2个碳原子,其(x+
| y |
| 4 |
B、H2C═C═O分子含有2个碳原子(x+
| y |
| 4 |
| z |
| 2 |
C、CH3CHO分子含有2个碳原子,(x+
| y |
| 4 |
| z |
| 2 |
D、CH3COOH分子含有2个碳原子(x+
| y |
| 4 |
| z |
| 2 |
故选BD.
点评:本题考查有机物燃烧分子式的确定,题目难度中等,注意根据原子守恒判断分子中碳原子数目及耗氧量规律,利用代入法验证.

练习册系列答案
相关题目
下列说法正确的是( )
| A、同种元素组成的物质一定是单质 |
| B、金属氧化物一定是碱性氧化物 |
| C、碱性氧化物一定是金属氧化物 |
| D、非金属氧化物一定是酸性氧化物 |
在下列各组物质中,分子数相同的一组是( )
| A、2L一氧化碳和2L二氧化碳 |
| B、18g水和标准状况下22.4L二氧化碳 |
| C、标准状况下22.4L水和lmol氧气 |
| D、0.2mol氢气和2.24L氯化氢气体 |
根据现行元素周期表的排布规律,如果第七周期排满,下列预测正确的是( )
| A、第七周期共有50种元素 |
| B、第七周期最后一种元素不与任何物质发生反应 |
| C、第七周期ⅦA族元素的原子在化学反应中可以得到1个电子 |
| D、第七周期任何一种元素的原子最外层上不超过8个电子 |
化学用语是学习化学的工具和基础.下列有关化学用语的使用正确的是( )
| A、用食醋除去水壶内的水垢:CaCO3+2H+=Ca2++CO2↑+H2O | ||||
| B、表示HS-电离的方程式为:HS-+H2O?S2-+H3O+ | ||||
C、用两个铁电极电解氢氧化钠溶液:2H2O
| ||||
| D、表示氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1)△H=+571.6 KJ?mol-1 |
下列叙述正确的是( )
| A、需要加热的化学反应都是吸热反应 |
| B、热化学方程式中各物质前的化学计量数不表示分子数 |
| C、在101KPa时1mol物质燃烧时的反应热叫做该物质的燃烧热 |
| D、如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应时放热反应 |
下列电子转移的表示方法中正确的是( )
A、 |
B、 |
C、 |
D、 |
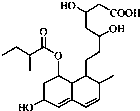 普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )| A、能与FeCl3溶液发生显色反应 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加成、取代、消去反应 |
| D、1mol该物质最多可与1molNaOH反应 |
 硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一.
硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一.