题目内容
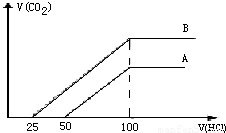
取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示.(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) 加入盐酸后产生CO2体积的最大值 ml,滴入盐酸的过程中发生反应的离子方程式 、 .
(2)曲线B 表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) ,两溶质物质的量之比为 ;加入盐酸后产生CO2体积的最大值为 ml.
(3)求原NaOH溶液物质的量的浓度 mol?L-1.
【答案】分析:(1)当生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,对于A溶液来说,滴加盐酸50mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,根据消耗盐酸的体积相等,说明所得溶液中的溶质为Na2CO3,根据反应的离子方程式计算;
(2)NaHCO3全部反应生成气体消耗的盐酸的体积大于生成NaHCO3消耗盐酸的体积,说明溶质为Na2CO3、NaHCO3,根据有关反应的离子方程式计算;
(3)根据Na元素守恒计算.
解答:解:(1)当生成CO2气体时,发生反应:HCO3-+H+=H2O+CO2↑,对于A溶液来说,滴加盐酸50mL时没有气体生成,可能发生
OH-+H+=H2O和CO32-+H+=HCO3-,
根据反应HCO3-+H+=H2O+CO2↑,可知n(HCO3-)=n(H+)=0.05L×0.1mol/L=0.005mol,
根据反应CO32-+H+=HCO3-,可知n(CO32-)=n(HCO3-)=0.005mol,而此时消耗n(H+)=0.05L×0.1mol/L=0.005mol,
则说明所得溶液中的溶质为Na2CO3,
HCO3-+H+=H2O+CO2↑
1mol 22.4L
0.005mol V
生成CO2体积为V=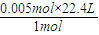 =0.112L=112mL,
=0.112L=112mL,
故答案为:Na2CO3;112;CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑;
(2)NaHCO3全部反应生成气体消耗的盐酸的体积大于生成NaHCO3消耗盐酸的体积,说明溶质为Na2CO3、NaHCO3,
设混合物中含有xmolNa2CO3,ymolNaHCO3,
则 CO32-+H+=HCO3-
1 1
n(CO32-) 0.025L×0.1mol/L
n(Na2CO3)=n(CO32-)=0.025L×0.1mol/L=0.0025mol,
又:HCO3-+H+=H2O+CO2↑
1 1 1
n(HCO3-) 0.075L×0.1mol/L
n(HCO3-)=0.075L×0.1mol/L=0.0075mol
所以:n(NaHCO3)=0.0075mol-0.0025mol=0.05mol,
所以:n(Na2CO3):n(NaHCO3)=0.0025mol:0.005mol=1:2,
n(CO2)=n(NaHCO3)=0.0075mol
V(CO2)=0.0075mol×22.4L/mol=0.168L=168mL,
故答案为:Na2CO3、NaHCO3;1:2; 168;
(3)根据Na元素守恒,反应后溶液的溶质为NaCl,则
n(NaOH)=n(HCl)=0.1L×0.1mol/L=0.01mol,
则c(NaOH)=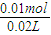 =0.5mol/L,
=0.5mol/L,
故答案为:0.5.
点评:本题考查混合物的计算,题目难度较大,本题关键是根据图象判断溶液溶质的成分,结合离子方程式利用守恒定律计算.
(2)NaHCO3全部反应生成气体消耗的盐酸的体积大于生成NaHCO3消耗盐酸的体积,说明溶质为Na2CO3、NaHCO3,根据有关反应的离子方程式计算;
(3)根据Na元素守恒计算.
解答:解:(1)当生成CO2气体时,发生反应:HCO3-+H+=H2O+CO2↑,对于A溶液来说,滴加盐酸50mL时没有气体生成,可能发生
OH-+H+=H2O和CO32-+H+=HCO3-,
根据反应HCO3-+H+=H2O+CO2↑,可知n(HCO3-)=n(H+)=0.05L×0.1mol/L=0.005mol,
根据反应CO32-+H+=HCO3-,可知n(CO32-)=n(HCO3-)=0.005mol,而此时消耗n(H+)=0.05L×0.1mol/L=0.005mol,
则说明所得溶液中的溶质为Na2CO3,
HCO3-+H+=H2O+CO2↑
1mol 22.4L
0.005mol V
生成CO2体积为V=
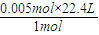 =0.112L=112mL,
=0.112L=112mL,故答案为:Na2CO3;112;CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑;
(2)NaHCO3全部反应生成气体消耗的盐酸的体积大于生成NaHCO3消耗盐酸的体积,说明溶质为Na2CO3、NaHCO3,
设混合物中含有xmolNa2CO3,ymolNaHCO3,
则 CO32-+H+=HCO3-
1 1
n(CO32-) 0.025L×0.1mol/L
n(Na2CO3)=n(CO32-)=0.025L×0.1mol/L=0.0025mol,
又:HCO3-+H+=H2O+CO2↑
1 1 1
n(HCO3-) 0.075L×0.1mol/L
n(HCO3-)=0.075L×0.1mol/L=0.0075mol
所以:n(NaHCO3)=0.0075mol-0.0025mol=0.05mol,
所以:n(Na2CO3):n(NaHCO3)=0.0025mol:0.005mol=1:2,
n(CO2)=n(NaHCO3)=0.0075mol
V(CO2)=0.0075mol×22.4L/mol=0.168L=168mL,
故答案为:Na2CO3、NaHCO3;1:2; 168;
(3)根据Na元素守恒,反应后溶液的溶质为NaCl,则
n(NaOH)=n(HCl)=0.1L×0.1mol/L=0.01mol,
则c(NaOH)=
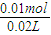 =0.5mol/L,
=0.5mol/L,故答案为:0.5.
点评:本题考查混合物的计算,题目难度较大,本题关键是根据图象判断溶液溶质的成分,结合离子方程式利用守恒定律计算.

练习册系列答案
相关题目
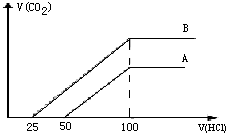 取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示.
取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示. 取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
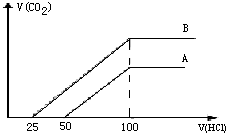 取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示.
取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的体积(单位为ml)的关系如图所示.