题目内容
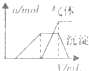
 取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:(1)原NaOH溶液的物质的量浓度为
0.75mol/L
0.75mol/L
.(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
NaOH、Na2CO3
NaOH、Na2CO3
,其物质的量之比为3:1
3:1
.(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为
112
112
mL.分析:(1)加入75ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液,根据氯离子、钠离子守恒,计算出氢氧化钠的物质的量,再根据物质的量浓度的定义计算;
(2)由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,计算碳酸氢钠的物质的量,再结合氢氧化钠的物质的量判断二氧化碳与氢氧化钠发生的反应,据此计算;
(3)由曲线B可知从25ml到75ml为碳酸氢钠与盐酸反应生成二氧化碳,据此计算.
(2)由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,计算碳酸氢钠的物质的量,再结合氢氧化钠的物质的量判断二氧化碳与氢氧化钠发生的反应,据此计算;
(3)由曲线B可知从25ml到75ml为碳酸氢钠与盐酸反应生成二氧化碳,据此计算.
解答:解:(1)加入75ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液.根据氯离子、钠离子守恒,
所以n(NaOH)=n(NaCl)=n(HCl)=0.075ml×0.1mol/L=0.0075mol,
所以c(NaOH)=
=0.75mol/L,
故答案为:0.75mol/L;
(2)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,
当n(CO2):n(NaOH)≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;
当
<n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当n(CO2):n(NaOH)≤
,反应按②进行,等于
,时,CO2、NaOH恰好反应生成Na2CO3;小于
时,生成Na2CO3,NaOH有剩余;
由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,
所以n(NaHCO3)=n(HCl)=(0.075-0.06)L×0.1mol/L=1.5×10-3mol,
根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×10-3mol,
由(1)可知,n(NaOH)=0.0075mol,
所以n(CO2):n(NaOH)=1.5×10-3mol:0.0075mol=1:5,小于1:2,所以反应按②进行,NaOH有剩余,溶液中溶质为Na2CO3和NaOH.
根据C原子守恒,所以n(Na2CO3)=n(CO2)=1.5×10-3mol,
再根据钠离子守恒,得溶液中氢氧化钠的物质的量为0.0075mol-1.5×10-3mol×2=0.0045mol,
所以溶液中NaOH与Na2CO3的物质的量之比为0.0045mol:1.5×10-3mol=3:1.
故答案为:NaOH、Na2CO3;3:1;
(3)由曲线B可知从25ml到75ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,
所以n(CO2)=n(HCl)=(0.075ml-0.025ml)×0.1mol/L=0.005mol,
所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL,
故答案为:112.
所以n(NaOH)=n(NaCl)=n(HCl)=0.075ml×0.1mol/L=0.0075mol,
所以c(NaOH)=
| 0.0075mol |
| 0.01L |
故答案为:0.75mol/L;
(2)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,
当n(CO2):n(NaOH)≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;
当
| 1 |
| 2 |
当n(CO2):n(NaOH)≤
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,
所以n(NaHCO3)=n(HCl)=(0.075-0.06)L×0.1mol/L=1.5×10-3mol,
根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×10-3mol,
由(1)可知,n(NaOH)=0.0075mol,
所以n(CO2):n(NaOH)=1.5×10-3mol:0.0075mol=1:5,小于1:2,所以反应按②进行,NaOH有剩余,溶液中溶质为Na2CO3和NaOH.
根据C原子守恒,所以n(Na2CO3)=n(CO2)=1.5×10-3mol,
再根据钠离子守恒,得溶液中氢氧化钠的物质的量为0.0075mol-1.5×10-3mol×2=0.0045mol,
所以溶液中NaOH与Na2CO3的物质的量之比为0.0045mol:1.5×10-3mol=3:1.
故答案为:NaOH、Na2CO3;3:1;
(3)由曲线B可知从25ml到75ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,
所以n(CO2)=n(HCl)=(0.075ml-0.025ml)×0.1mol/L=0.005mol,
所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL,
故答案为:112.
点评:本题考查混合物的有关计算,难度中等,关键根据图中盐酸的体积计算出NaOH、CO2的物质的量,判断CO2与NaOH反应过程.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
在理解概念的基础上,理清概念之间的相互关系,构建知识网络是学习化学的重要方法,如图是中学化学常见化学概念之间的相互关系.
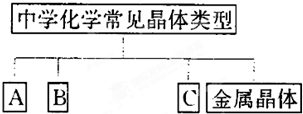
(1)完成下表,且实例按以下要求填写.
①只能由 H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3).
(2)取上述表格中A、B、C三种晶体中某一晶体溶于水得W溶液,写出等物质的量浓度等体积的硫酸氢钠与W溶液反应的离子方程式 ;
(3)写出上述表格中熔点最高的物质与氢氧化钠反应的化学方程式: .

(1)完成下表,且实例按以下要求填写.
①只能由 H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3).
| A | B | C | ||
| 晶体类别 | 金属晶体 | |||
| 实例的化学式 | Na |
(3)写出上述表格中熔点最高的物质与氢氧化钠反应的化学方程式:
在理解概念的基础上,理清概念之间的相互关系,构建知识网络是学习化学的重要方法,下图是中学化学常见化学概念之间的相互关系。
 |
(1) 完成下表,且实例按以下要求填写。
①只能由H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3)。
A | B | C | ||
晶体类别 | 金属晶体 | |||
实例的化学式 | Na |
(2)取上述表格中A、B、C三种晶体中某一晶体溶于水得W溶液,写出等物质的量浓度等体积的硫酸氢钠与W溶液反应的离子方程式 ;
(3)写出上述表格中熔点最高的具体物质与氢氧化钠反应的化学方程式 。
![]()