题目内容
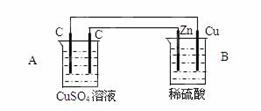
将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如下图的装置:(以下均假设反应过程中溶液体积不变)。
(1)铁片上的电极反应式为 。
(2)铜片周围溶液会出现 的现象。
(3)若2 min后测得铁片和铜片之间的质量差为1.2g,计算导线中流过的电子的物质的量为 mo1。
(1)Fe -2e-= Fe2+ (2)溶液颜色变浅 (3)0.02
解析试题分析:(1)Fe、Cu及硫酸铜溶液构成了原电池,由于活动性Fe>Cu,所以Fe作负极,发生反应Fe-2e-= Fe2+。(2)由于Cu2+不断在铜片上放电,Cu2++2e-=Cu。所以铜片周围溶液中Cu2+的浓度降低,溶液的颜色会出现变浅。(3)总反应方程式是Fe+Cu2+=Fe2++Cu。可见每有2mol的电子转移,在铁片和铜片之间的质量差56g+64g=120g,现在质量差值为1.2g,,所以电子转移(1.2g÷120g)×2=0.02mol..
考点:考查原电池反应原理、相应的现象及电子转移的知识。

练习册系列答案
相关题目
某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| ① | Mg 、Al | 稀盐酸 | 偏向Al |
| ② | Al、Cu | 稀盐酸 | 偏向Cu |
| ③ | Al、石墨 | 稀盐酸 | 偏向石墨 |
| ④ | Mg、Al | NaOH溶液 | 偏向Mg |
| ⑤ | Al、Zn | 浓硝酸 | 偏向Al |
根据上表中的实验现象完成下列问题:
(1)实验①、②中Al所作的电极是否相同?
答:____________________________________________
(2)写出实验③中的电极名称、电极反应式和电池总反应方程式。铝为( )______________________________
石墨为( )__________________________
电池总反应:__________________________
(3)实验④中的铝作________极。
(4)实验⑤中铝作________极。