题目内容
在化学平衡体系中,如果下列各选项的量发生变化,其中一定能表示平衡移动的是
- A.反应混合物的浓度
- B.反应物的转化率
- C.正逆反应速度
- D.反应混合物的压强

(10分)天然气的主要成分是甲烷。在某平衡体系中存在CH4、H2O、CO、H2四种气体,
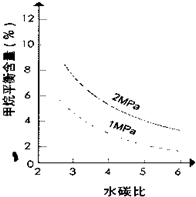
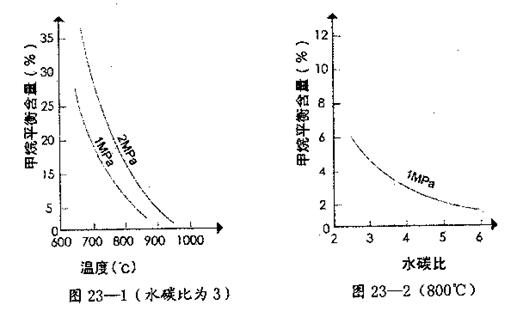
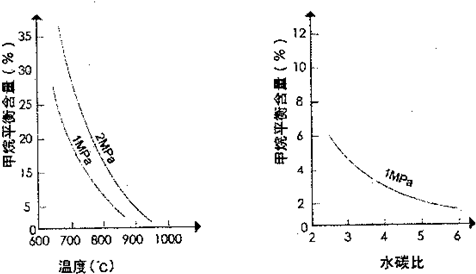
其平衡常数表达式为 。已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷转化反应的影响如下图:
。已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷转化反应的影响如下图:
请回答下列问题:
(1)写出该可逆反应的化学方程式:
(2)根据图23—1判断△H 0,△S 0(选填“>”、“<”或“=”)。
(3)假设上述反应在恒容、恒温下进行,判断反应达到平衡状态时的标志是
| A.CO减少的化学反应速率和H2O(曲减少的化学反应速率相等 |
| B.CO、H2O(g)、CH4、H2的浓度都相等 |
| C.CO、H20(g)、CH4、H2的浓度都不再发生变化 |
| D.正、逆反应速率都为零 |
下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:

(1)已知该产业链中某反应的平衡表达式为:K=
它所对应反应的化学方程式为 。
已知在一定温度下,在同一平衡体系中各反应的平衡常数如下:
C(s)+CO2(g)  2CO(g),K1
2CO(g),K1
CO(g)+H2O(g)  H2(g)+CO2(g),K2
H2(g)+CO2(g),K2
C(s)+H2O(g)  CO(g)+H2(g),K3
CO(g)+H2(g),K3
则K1、K2、K3之间的关系为 。
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
|
温度/℃ |
400 |
500 |
800 |
|
平衡常数K |
9.94 |
9 |
1 |
该反应的逆反应方向是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时CO的转化率为 。
(3)对于反应N2O4(g) 2NO2(g)-Q(Q>0),在温度
2NO2(g)-Q(Q>0),在温度
为T1、T2时,平衡体系中NO2的体积分数随压强变化
曲线如图所示。下列说法正确的是 。

A.两种不同的温度比较:T1 > T2
B.A、C两点的反应速率:A<C
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法实现
(4)如右图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率,反应原理为:NO(g) + NO2(g) + 2NH3(g)  2N2(g) + 3H2O(g)
2N2(g) + 3H2O(g)

以下说法正确的是(注:脱氮率即氮氧化物转化率)
A.上述反应的正反应为吸热反应
B.相同条件下,改变压强对脱氮率没有影响
C.曲线①、②最高点表示此时平衡转化率最高
D.催化剂①、②分别适合于250℃和450℃左右脱氮
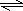 CO(g)+3H2(g)
CO(g)+3H2(g)