题目内容
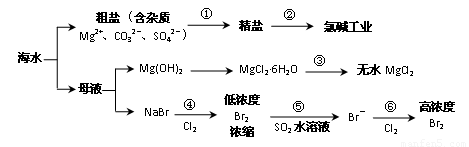
根据下图海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗0.1mol Cl2
D.过程⑤在生产中无需解决其对金属设备的腐蚀问题
【答案】
C
【解析】
试题分析:A、粗盐通过加入氯化钡、碳酸钠、氢氧化钠等物质除去杂质,是化学变化,错误;B、因为MgCl2水解,在灼烧MgCl2·6H2O得到MgO,需要在HCl氛围下加热才能得到无水MgCl2,错误;C、正确;D、SO2与Br2反应为SO2+Br2+H2O=H2SO4+HBr,产生的酸会腐蚀设备,需做防腐处理。
考点:考查工业流程有关问题。

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
根据下图海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2?6H2O受热生成Mg(OH)Cl和HCl气体等.( )

已知:MgCl2?6H2O受热生成Mg(OH)Cl和HCl气体等.( )
| A、氯碱工业中电解饱和食盐水是一个将化学能转化为电能的过程 | B、在过程③中将MgCl2?6H2O灼烧即可制得无水MgCl2 | C、在过程④、⑥反应中每氧化0.2 mol Br- 需消耗0.1mol Cl2 | D、过程⑤在生产中无需解决其对金属设备的腐蚀问题 |