题目内容
A、B两种金属以原子个数之比1∶2相混合,混合物共11.9g,加入足量盐酸反应后,产生标准状况时的氢气8.96L,A转化为 、B转化为
、B转化为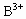 .又已知A的相对原子质量为B的相对原子质量的2.41倍,试计算A、B两种金属的相对原子质量.
.又已知A的相对原子质量为B的相对原子质量的2.41倍,试计算A、B两种金属的相对原子质量.
答案:
解析:
解析:
|
提示: 据已知条件A、B二种金属原子个数之比以及相对原子质量之比,便可求知二种金属的质量比.根据混合物总质量,可求出A、B的质量分别为6.5g、5.4g 已知A、B原子数比为1∶2 所以A、B分别跟盐酸反应产生 据题意,产生的 所以B与盐酸反应放出 则A的相对原子质量为27×2.41=65 |

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目

 的物质的量之比为1∶3
的物质的量之比为1∶3
 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol