题目内容
10.N2O3中N元素的化合价为( )| A. | +3 | B. | +5 | C. | +4 | D. | +6 |
分析 根据在化合物中正负化合价代数和为零,结合物质的化学式进行解答本题.
解答 解:氧元素显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×3=0,则x=+3价.
故选:A.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
20.用下列装置能达到有关实验目的是( )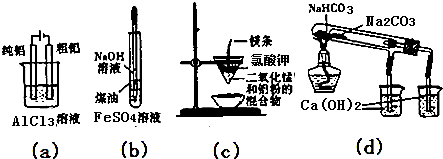

| A. | 用图(a)装置电解精炼铝 | |
| B. | 用图(b)装置制备Fe(OH)2 | |
| C. | 图(c)装置可制得金属钾 | |
| D. | 图(d)验证NaHCO3和Na2CO3的热稳定性 |
5.已知在448℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数为49.下列叙述中正确的是(相同温度下)( )
| A. | 反应H2(g)+I2(g)?2HI(g)的平衡常数K=$\frac{c(HI)}{c({H}_{2})c({I}_{2})}$=49 | |
| B. | 反应2HI(g)?H2(g)+I2(g)的平衡常数K=$\frac{c({H}_{2})c({I}_{2})}{{c}^{2}(HI)}$=49 | |
| C. | 反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数K=$\frac{c({H}_{2})c({I}_{2})}{{c}^{2}(HI)}$=7 | |
| D. | 反应2HI(g)?H2(g)+I2(g)的平衡常数K=$\frac{c({H}_{2})c({I}_{2})}{{c}^{2}(HI)}$=$\frac{1}{49}$ |
15.将绿豆大小的金属钠投入加有酚酞的100mL蒸馏水中,则( )
| A. | 溶液变蓝 | B. | Na浮在水面上并熔化成小球 | ||
| C. | Na在水面上游动 | D. | 有H2生成 |
2.除去如表物质中的杂质(括号内为杂质,所选用的试剂及操作方法均正确的一组是( )
| 选项 | 被提纯的物质 | 选用试剂 | 操作方法 |
| A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
| B | CuSO4(H2SO4) | NaOH溶液 | 过滤 |
| C | CO2(CO) | 氧气 | 点燃 |
| D | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
19.向纯水中加入下列物质,对水的电离平衡几乎没有影响的是( )
| A. | 硫酸钠 | B. | 氨水 | C. | 醋酸 | D. | 盐酸 |
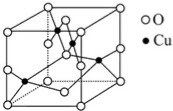 太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等.回答下列问題:
太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等.回答下列问題: 呵护生存环境,共建和谐社会.
呵护生存环境,共建和谐社会.