题目内容
有下列五组物质:A、O2和O3 B、37Cl和35Cl C、CH4与C7H16D、CH3CH2CH2CH3与
(1) 组两种物质互为同位素;
(2) 组两种物质互为同素异形体;
(3) 组两种物质互为同系物;
(4) 组两种物质互为同分异构体.

(1)
(2)
(3)
(4)
考点:同位素及其应用,同素异形体,芳香烃、烃基和同系物,同分异构现象和同分异构体
专题:
分析:根据结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;分子式相同,结构不同的化合物互称为同分异构体;质子数相同中子数不同的原子互称同位素;同种元素形成的不同单质互为同素异形体来解答.
解答:
解:(1)3517Cl和3717Cl 中子数不同,是氯元素的不同原子,互为同位素,故选:B;
(2)O2和O3是氧元素组成的结构不同的单质,互为同素异形体,故选:A;
(3)CH4与C7H16 结构相似,都属于烷烃,分子组成相差2个CH2原子团,互为同系物,故选:C;
(4)CH3CH2CH2CH3 与 ,分子式相同,结构不同,为同分异构体,故选:D.
,分子式相同,结构不同,为同分异构体,故选:D.
(2)O2和O3是氧元素组成的结构不同的单质,互为同素异形体,故选:A;
(3)CH4与C7H16 结构相似,都属于烷烃,分子组成相差2个CH2原子团,互为同系物,故选:C;
(4)CH3CH2CH2CH3 与
 ,分子式相同,结构不同,为同分异构体,故选:D.
,分子式相同,结构不同,为同分异构体,故选:D.
点评:本题考查基本概念,明确同位素、同素异形体、同分异构体等概念的要点即可解答,难度不大,注重对学生基础知识的考查.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
有机物A的结构简式为 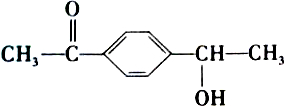 ,有关它的说法正确的是( )
,有关它的说法正确的是( )
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A、A遇FeCl3溶液显紫色 |
| B、A被酸性KMnO4溶液氧化可生成羧酸 |
| C、乙酸与A形成的酯的化学式是C12H14O3 |
| D、A能发生取代、加成、消去、氧化、聚合等反应 |
下列各组元素中按微粒半径递增顺序排列的是( )
| A、K、Na、Li |
| B、Ba2+、Ca2+、Mg2+? |
| C、N、O、F |
| D、Ca2+、K+、Cl- |
下列说法中正确的是( )
| A、元素性质的周期性变化是指原子半径、元素的主要化合价及原子核外电子排布的周期性变化 |
| B、元素性质的周期性变化决定于元素原子结构的周期性变化 |
| C、从Li→F,Na→Cl,元素的最高化合价均呈现从+1价→+7价的变化 |
| D、电子层数相同的原子核外电子排布,其最外层电子数均从1个到8个呈现周期性变化 |
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: | ||
B、NH4Cl的电子式: +Cl- +Cl- | ||
C、原子核内有8个中子的氧原子:
| ||
| D、二氧化碳的结构式 O-C-O |
属于联合制碱法优点的是( )
| A、氨和二氧化碳由合成氨厂提供 |
| B、母液可回收氯化铵 |
| C、氯化钠的利用率达96%以上 |
| D、以上全是 |
 0mol.L-1NaHSO3(含少量淀粉)10.0mL和0.020mol.L-1KIO3(过量)酸性溶液40.0mL混合(混合后体积变化忽略不计),在如下不同温度下分别进行实验,记录从反应开始到溶液变蓝所需时间,实验数据如下表:
0mol.L-1NaHSO3(含少量淀粉)10.0mL和0.020mol.L-1KIO3(过量)酸性溶液40.0mL混合(混合后体积变化忽略不计),在如下不同温度下分别进行实验,记录从反应开始到溶液变蓝所需时间,实验数据如下表: