题目内容
| |||||||||||||||||||||||||||
解析:
(1) |
答案:D 解析:CuCl2与CuSO4溶液中均含有Cu2+,但CuSO4溶液不与铝片反应.故铝片与CuCl2溶液的反应一定是Cl-起到了破坏铝表面氧化物薄膜的作用. CuCl2中的Cl-破坏掉氧化膜以后,Al能置换出CuCl2溶液中的Cu而使铝片表面呈暗红色,反应方程式为:2Al+3Cu2+ 因此设法除去铝表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使铝片与CuSO4溶液发生反应. |
(2) |
答案:Cu 解析:CuCl2与CuSO4溶液中均含有Cu2+,但CuSO4溶液不与铝片反应.故铝片与CuCl2溶液的反应一定是Cl-起到了破坏铝表面氧化物薄膜的作用. CuCl2中的Cl-破坏掉氧化膜以后,Al能置换出CuCl2溶液中的Cu而使铝片表面呈暗红色,反应方程式为:2Al+3Cu2+ 因此设法除去铝表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使铝片与CuSO4溶液发生反应. |
(3) |
答案:H2 ①随着反应的进行生成铝离子浓度增大,水解程度增大,产生H+的浓度增大,②该反应放热,升高温度反应加快,③铜与铝构成原电池,加快铝溶解 解析:CuCl2与CuSO4溶液中均含有Cu2+,但CuSO4溶液不与铝片反应.故铝片与CuCl2溶液的反应一定是Cl-起到了破坏铝表面氧化物薄膜的作用. CuCl2中的Cl-破坏掉氧化膜以后,Al能置换出CuCl2溶液中的Cu而使铝片表面呈暗红色,反应方程式为:2Al+3Cu2+ 因此设法除去铝表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使铝片与CuSO4溶液发生反应. |
(4) |
CuCl2与CuSO4溶液中均含有Cu2+,但CuSO4溶液不与铝片反应.故铝片与CuCl2溶液的反应一定是Cl-起到了破坏铝表面氧化物薄膜的作用. CuCl2中的Cl-破坏掉氧化膜以后,Al能置换出CuCl2溶液中的Cu而使铝片表面呈暗红色,反应方程式为:2Al+3Cu2+ 因此设法除去铝表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使铝片与CuSO4溶液发生反应. |

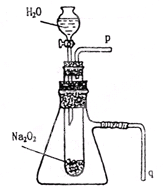 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来. Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4mL 0.01mol?L-1KMnO4溶液与2mL 0.1mol?L-1 H2C2O4溶液进行实验,改变条件如下:
Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4mL 0.01mol?L-1KMnO4溶液与2mL 0.1mol?L-1 H2C2O4溶液进行实验,改变条件如下: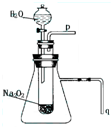 有演示实验:用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
有演示实验:用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.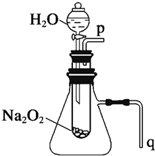 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.