题目内容
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
| “嫦娥一号”发射火箭燃料 | 液氢 (H2) | ①2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1 ②2H2(l)+O2(l)=2H2O(g) △H=-482.6kJ·mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g)△H=-2013.8kJ·mol-1 ④ C3H8(g)+5O2(g) =3CO2(g)+4H2O(l)△H=-2221.5kJ·mol-1 |
- A.571.6 kJ·mol-1,2221.5kJ·mol-1
- B.241.3 kJ·mol-1,2013.8 kJ·mol-1
- C.285.8 kJ·mol-1,2013.8 kJ·mol-1
- D.285.8 kJ·mol-1,2221.5 kJ·mol-1
D
燃烧热是指在常温常压下,1mol纯物质完全燃烧生成稳定的氧化物时所放出的能量叫做该物质的燃烧热,所以,氢气和丙烷的燃烧热分别为285.8 kJ·mol-1,2221.5 kJ·mol-1;正确选项为D;
燃烧热是指在常温常压下,1mol纯物质完全燃烧生成稳定的氧化物时所放出的能量叫做该物质的燃烧热,所以,氢气和丙烷的燃烧热分别为285.8 kJ·mol-1,2221.5 kJ·mol-1;正确选项为D;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
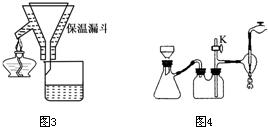 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.