题目内容
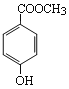
【题目】利用![]() 和
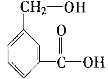
和![]() 制备
制备![]() 的原理为:
的原理为:
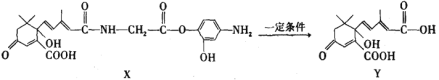
①![]()
②![]()
已知:A、B均为有机物,两个反应均能自发进行;NA代表阿伏加德罗常数。下列说法正确的是
A.B为![]() 和
和![]() 制备
制备![]() 的催化剂
的催化剂
B.1mol![]() 与足量的B在一定条件下发生反应②,共转移2NA个电子
与足量的B在一定条件下发生反应②,共转移2NA个电子
C.反应①的反应物的总能量大于产物的总能量
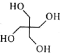
D.标准状况下,22.4L![]() 含NA个分子
含NA个分子
【答案】C
【解析】
A.B为中间产物,A在反应前后性质和质量不变,为![]() 和
和![]() 制备
制备![]() 的催化剂,A错误;
的催化剂,A错误;
B.根据反应方程式可知,氧元素由0价变为-1价,但其它元素化合价如何变化并不明确,故1mol![]() 与足量的B在一定条件下发生反应②,转移的电子数无法确定,B错误;
与足量的B在一定条件下发生反应②,转移的电子数无法确定,B错误;
C.反应①的![]() ,该反应能自发进行,则
,该反应能自发进行,则![]() ,故
,故![]() <0,反应物的总能量大于产物的总能量,C正确;
<0,反应物的总能量大于产物的总能量,C正确;
D.在标况下,![]() 为非气体状态,分子数无法确定,D错误;
为非气体状态,分子数无法确定,D错误;
答案选C。

【题目】一定温度下,在三个体积均为1.0 L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A.该反应的正方应为放热反应
B.达平衡时,容器Ⅱ中CH3OCH3的浓度大于0.16 mol/L
C.达平衡时,容器Ⅲ中![]() 比容器Ⅱ中的大
比容器Ⅱ中的大
D.若起始时向容器Ⅰ中充入CH3OH(g)0.30 mol、CH3OCH3(g)1.50 mol和H2O(g)0.30 mol,则反应将向逆反应方向进行
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
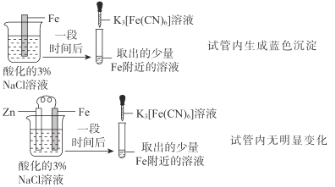
A |
| Zn保护了Fe不被腐蚀 |
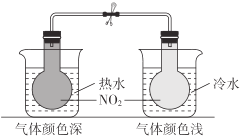
B |
| 2NO2(g)N2O4(g)为吸热反应 |
C |
| 木炭与浓硝酸发生了反应 |
D |
| 碳酸钠的水解程度强 |
A.AB.BC.CD.D