题目内容
关于相同体积、相同pH的盐酸和醋酸溶液及其相关实验的说法,正确的是( )
| A.室温时,由水电离出的c(H+):盐酸小于醋酸溶液 |
| B.用等浓度的NaOH溶液中和两种溶液时:所需体积相同 |
| C.均加水冲稀10倍后:盐酸的pH大于醋酸溶液的pH |
| D.均加入足量镁粉,反应完全后产生H2的物质的量:盐酸大于醋酸溶液 |
A.室温时,pH相等的盐酸和醋酸溶液中氢氧根离子浓度相等,所以由水电离出的c(H+)相等,故A错误;
B.相同体积、相同pH的盐酸和醋酸溶液,n(CH3COOH)>n(HCl),且盐酸和醋酸都是一元酸,所以用等浓度的NaOH溶液中和两种溶液时:盐酸所需体积小于醋酸所需体积,故B错误;
C.均加水冲稀10倍后,醋酸中氢离子浓度大于盐酸,所以盐酸的pH大于醋酸溶液的pH,故C正确;
D..相同体积、相同pH的盐酸和醋酸溶液,n(CH3COOH)>n(HCl),且盐酸和醋酸都是一元酸,所以均加入足量镁粉,反应完全后产生H2的物质的量:盐酸小于醋酸溶液,故D错误;
故选C.
B.相同体积、相同pH的盐酸和醋酸溶液,n(CH3COOH)>n(HCl),且盐酸和醋酸都是一元酸,所以用等浓度的NaOH溶液中和两种溶液时:盐酸所需体积小于醋酸所需体积,故B错误;
C.均加水冲稀10倍后,醋酸中氢离子浓度大于盐酸,所以盐酸的pH大于醋酸溶液的pH,故C正确;
D..相同体积、相同pH的盐酸和醋酸溶液,n(CH3COOH)>n(HCl),且盐酸和醋酸都是一元酸,所以均加入足量镁粉,反应完全后产生H2的物质的量:盐酸小于醋酸溶液,故D错误;
故选C.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
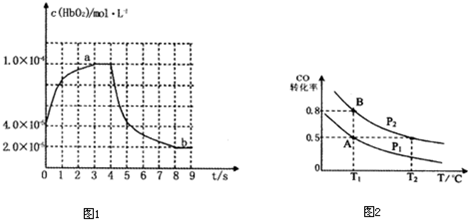
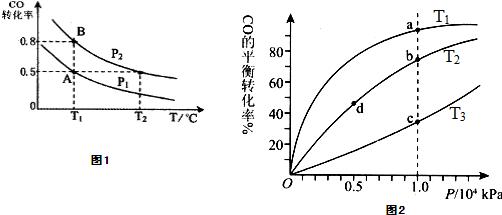
 CH3OH ( g ) △H =-90.8 kJ·mol-1 在一容积可变的 密闭容器中充入10 mol CO 和20 molH2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为20 L。
CH3OH ( g ) △H =-90.8 kJ·mol-1 在一容积可变的 密闭容器中充入10 mol CO 和20 molH2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为20 L。

 A.①表示化学反应H2(g)+Cl2(g)
=2HCl(g)的能量变化,则该反应的反应热△H =183 j/mol
A.①表示化学反应H2(g)+Cl2(g)
=2HCl(g)的能量变化,则该反应的反应热△H =183 j/mol 2C(g)+6D在不同压强下B%随时间的变化,则D一定是气体
2C(g)+6D在不同压强下B%随时间的变化,则D一定是气体
 B.②表示其它条件不变时,反应4A(g)+3B(g)
2C(g)+6D在不同压强下B%随时间的变化,则D-定是气体
B.②表示其它条件不变时,反应4A(g)+3B(g)
2C(g)+6D在不同压强下B%随时间的变化,则D-定是气体