题目内容
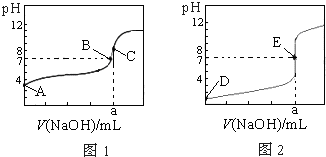 如图为常温下用0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1盐酸和20.00mL 0.1000mol?L-1醋酸的曲线.若以HA表示酸,下列判断和说法正确的是( )
如图为常温下用0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1盐酸和20.00mL 0.1000mol?L-1醋酸的曲线.若以HA表示酸,下列判断和说法正确的是( )| A、图1是滴定盐酸的曲线 | B、B、E状态时,两溶液中离子浓度均为c(Na+)=c(A-) | C、C、E状态时,反应消耗的酸n(CH3COOH)=n(HCl) | D、当0 mL<V(NaOH)<20.00 mL时,对应溶液中各离子浓度大小顺序一定均为c(A-)>c(Na+)>c(H+)>c(OH-) |
分析:A、根据盐酸和醋酸在滴定开始时的pH来判断;
B、根据溶液中的电荷守恒来判断;
C、根据酸和碱反应的化学方程式来计算回答;
D、根据氢氧化钠和醋酸以及盐酸反应的原理结合给定的物质的量计算来回答.
B、根据溶液中的电荷守恒来判断;
C、根据酸和碱反应的化学方程式来计算回答;
D、根据氢氧化钠和醋酸以及盐酸反应的原理结合给定的物质的量计算来回答.
解答:解:A、滴定开始时0.1000mol/L盐酸pH=1,0.1000mol/L醋酸pH>1,所以滴定盐酸的曲线是图1,故A错误;
B、达到B、E状态时,溶液是中性的,此时c(H+)=c(OH-),根据电荷守恒,则两溶液中离子浓度均为 c(Na+)=c(A-),故B正确;
C、达到C、E状态时,消耗的氢氧化钠物质的量是相等的,根据反应原理:HCl~NaOH,CH3COOH~NaOH,反应消耗的n(CH3COOH)=n(HCl),故C正确;
D、当0 mL<V(NaOH)<20.00 mL时,酸相对于碱来说是过量的,所得溶液是生成的盐和酸的混合物,假设当加入的氢氧化钠极少量时,生成了极少量的钠盐(氯化钠或是醋酸钠),剩余大量的酸,此时c(A-)>c(H+)>c(Na+)>c(OH-),故D错误.
故选BC.
B、达到B、E状态时,溶液是中性的,此时c(H+)=c(OH-),根据电荷守恒,则两溶液中离子浓度均为 c(Na+)=c(A-),故B正确;
C、达到C、E状态时,消耗的氢氧化钠物质的量是相等的,根据反应原理:HCl~NaOH,CH3COOH~NaOH,反应消耗的n(CH3COOH)=n(HCl),故C正确;
D、当0 mL<V(NaOH)<20.00 mL时,酸相对于碱来说是过量的,所得溶液是生成的盐和酸的混合物,假设当加入的氢氧化钠极少量时,生成了极少量的钠盐(氯化钠或是醋酸钠),剩余大量的酸,此时c(A-)>c(H+)>c(Na+)>c(OH-),故D错误.
故选BC.
点评:本题考查NaOH与CH3COOH、盐酸的反应,涉及盐类的水解和溶液离子浓度的大小比较知识,注意利用电荷守恒的角度做题.

练习册系列答案
相关题目