题目内容
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )
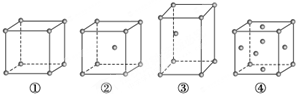

分析:A.②属于钾、钠和铁型,③属于镁、锌、钛型;
B.利用均摊法计算;
C.③中的配位数是12;
D.空间利用率③=④.
B.利用均摊法计算;
C.③中的配位数是12;
D.空间利用率③=④.
解答:解:A.②是体心立方堆积,属于钾、钠和铁型,③是六方最密堆积,属于镁、锌、钛型,故A错误;
B.利用均摊法计算原子个数,①中原子个数=8×
=1,②中原子个数=1+8×
=2,③中原子个数=1+8×
=2,④中原子个数=8×
+6×
=4,故B正确;
C.③中的配位数是12,故C错误;
D.①中空间利用率为51%,②中空间利用率为68%,③④中空间利用率为74%,所以空间利用率大小关系为:①<②<③=④,故D错误;
故选B.
B.利用均摊法计算原子个数,①中原子个数=8×
| 1 |
| 8 |
| 1 |
| 8 |
| 1 |
| 8 |
| 1 |
| 8 |
| 1 |
| 2 |
C.③中的配位数是12,故C错误;
D.①中空间利用率为51%,②中空间利用率为68%,③④中空间利用率为74%,所以空间利用率大小关系为:①<②<③=④,故D错误;
故选B.
点评:本题考查了晶体结构,难度较大,注意典型晶体晶胞结构、配位数的计算、原子个数的计算,为学习难点.

练习册系列答案
相关题目


 键;D.
键;D. 键;E.p—p
键;E.p—p 键;F.
键;F. 键;G.
键;G. 键;H.
键;H.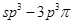 键
键