题目内容
下列原理所测的中和热最接近-57.3kJ/mol的是( )
| A、将标况下11.2L HCl气体通入50mL 0.01 mol/L NaOH溶液中反应 | B、用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L HNO3溶液反应 | C、用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L H2SO4溶液反应 | D、用55mL 0.01 mol/L NaOH溶液与50mL 0.01 mol/L HF溶液反应 |
分析:在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热.必须是酸和碱的稀溶液,因为浓酸溶液和浓碱溶液在相互稀释时会放热.
强酸和强碱的稀溶液反应才能保证H+(aq)+OH-(aq)=H2O(l)中和热均为57.3 kJ?mol-1,而弱酸或弱碱在中和反应中由于电离吸收热量,反应不能生成沉淀,生成沉淀会放出热量.
强酸和强碱的稀溶液反应才能保证H+(aq)+OH-(aq)=H2O(l)中和热均为57.3 kJ?mol-1,而弱酸或弱碱在中和反应中由于电离吸收热量,反应不能生成沉淀,生成沉淀会放出热量.
解答:解:A、标况下11.2L即0.5mol HCl气体通入50mL 0.01 mol/L NaOH溶液中反应,生成水的量小于1mol,放出的热量不足57.3KJ,所以中和热大于-57.3kJ/mol,故A错误;
B、用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L HNO3溶液反应,生成的水的物质的量是1mol,放出的热量是为57.3kJ,所以中和热等于-57.3kJ/mol,故B正确;
C、用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L H2SO4溶液反应,生成1mol水,且有硫酸钡沉淀生成,放出的热量比57.3kJ还要多,所以中和热小于-57.3kJ/mol,故C错误.
D、55mL 0.01 mol/L NaOH溶液与50mL 0.01 mol/L HF溶液反应,生成水的量小于1mol,并且HF酸是弱酸,电离需要吸热,所以中和热大于-57.3kJ/mol,故D错误.
故选B.
B、用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L HNO3溶液反应,生成的水的物质的量是1mol,放出的热量是为57.3kJ,所以中和热等于-57.3kJ/mol,故B正确;
C、用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L H2SO4溶液反应,生成1mol水,且有硫酸钡沉淀生成,放出的热量比57.3kJ还要多,所以中和热小于-57.3kJ/mol,故C错误.
D、55mL 0.01 mol/L NaOH溶液与50mL 0.01 mol/L HF溶液反应,生成水的量小于1mol,并且HF酸是弱酸,电离需要吸热,所以中和热大于-57.3kJ/mol,故D错误.
故选B.
点评:本题考查了中和热的数值和概念理解,反应过程中热量变化是解题关键,题目难度中等.

练习册系列答案
相关题目
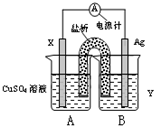 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题. 2CO2(g)+
N2(g)。△H<0
2CO2(g)+
N2(g)。△H<0

 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol 
