题目内容
【题目】常温下,将a mol/L的氨水滴入到20.00mL0.108mol/L的盐酸中,混合溶液的pH与氨水的体积(V)的关系如图所示。下列说法不正确的是( )

A.图上四点对应溶液中离子种类相同
B.图上四点对应的溶液中水的电离程度由大到小的顺序为N>P>M>Q
C.若N点为恰好反应点,则M点溶液中存在c(Cl-)=2c(NH3·H2O)+2c(NH4+)
D.若N点溶液中存在c(H+)=c(OH-)+c(NH3·H2O),则N点为滴定反应的恰好反应点
【答案】B
【解析】
A.根据题意,随着氨水的滴加,存在的离子均含有H+、Cl-、NH4+、OH-四种离子,A正确;
B.酸性或碱性越强,水的电离程度越小,故为P>N> M>Q,B错误;
C.若N点为恰好反应点,则M点溶液为NH4Cl、HCl等浓度的混合溶液,溶液中存在物料守恒,为c(Cl-)=2c(NH3·H2O)+2c(NH4+),C正确;
D.若N点溶液中存在c(H+)=c(OH-)+c(NH3·H2O),根据质子守恒,溶质为NH4Cl,则N点为滴定反应的恰好反应点,D正确;
故合理选项是B。

练习册系列答案
相关题目
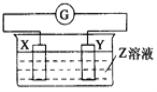
【题目】X、Y两根金属棒插入Z溶液中构成如图的装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是( )
选项 | X | Y | Z |
A | Zn | Cu | 稀硫酸 |
B | Cu | Zn | 稀硫酸 |
C | Cu | Ag | 硫酸铜溶液 |
D | Ag | Zn | 硝酸银溶液 |
A.AB. BC. CD. D