题目内容
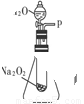
某化学实验小组拟用以下仪器测量锌与稀硫酸的反应速率(连接导管的橡皮管未画出)。

请完成下列问题:
(1)装置的连接顺序为: (填装置编号),B导管口应该与 导管口相连
(2)检查气密性是不可缺少的一步。检查该装置气密性的方法是:
(3)除图中所用仪器外,实验还需要的一种仪器是 ;图中③装置中的液体为
(4)测得经过50秒时量筒中液体的体积为25.0mL,则反应速率可表示为:
(5)为简化装置,提高效率,你对实验装置的修改建议是:
(1)①③④②;D(各1分,共2分)
(2)(连接好装置,)在量筒中加入适量水以没过导管口,用双手捂住烧瓶,若导管口有气泡冒出,则说明装置气密性良好。(2分)
(3)秒表;水(各1分,共2分)
(4)υ(H2)=0.5mL/s(2分)
(5)其他装置(仪器)不用,改用一个带有刻度的注射器与装置①相连。(2分)

练习册系列答案
相关题目
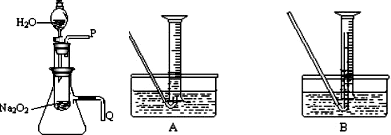 (2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来. (1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:
(1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:
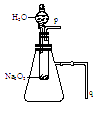 (1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是: