题目内容
氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用.
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H= .(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如下表所示:
已知:破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量.
①则T1 T2(填“>”、“<”或“=”)
②在T2K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)= ,平衡时N2的转化率α(N2)= .
③下列图象1分别代表焓变(△H)、混合气体平均相对分子质量(
)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 .
(3)某N2H4(肼或联氨)燃料电池(产生稳定、无污染的物质)原理如图2所示.
①M区发生的电极反应式为 .
②用上述电池做电源,用图3装置电解饱和氯化钾溶液(电极均为惰性电极),设饱和氯化钾溶液体积为500mL,当溶液的pH值变为13时(在常温下测定),若该燃料电池的能量利用率为80%,则需消耗N2H4的质量为 g(假设溶液电解前后体积不变).

(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如下表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1
②在T2K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=
③下列图象1分别代表焓变(△H)、混合气体平均相对分子质量(
. |
| M |
(3)某N2H4(肼或联氨)燃料电池(产生稳定、无污染的物质)原理如图2所示.
①M区发生的电极反应式为
②用上述电池做电源,用图3装置电解饱和氯化钾溶液(电极均为惰性电极),设饱和氯化钾溶液体积为500mL,当溶液的pH值变为13时(在常温下测定),若该燃料电池的能量利用率为80%,则需消耗N2H4的质量为

考点:物质的量或浓度随时间的变化曲线,用盖斯定律进行有关反应热的计算,原电池和电解池的工作原理,化学平衡的影响因素,化学平衡状态的判断
专题:化学反应中的能量变化,化学平衡专题,电化学专题
分析:(1)由①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×
得到4NH3(g)+3O2(g)=2N2(g)+6H2O(l);
(2)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
结合v=
及转化率计算;
③焓变(△H)始终不变,混合气体平均相对分子质量(
)为变量、N2体积分数φ(N2)为变量,气体密度(ρ)始终不变;
(3)①左端为负极,在酸性电解质中失去电子生成氮气和氢离子;
②该燃料电池的能量利用率为80%,即电池转移电子的80%=电解中转移电子,结合电子转移守恒计算.
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×
| 1 |
| 5 |
(2)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
结合v=
| △c |
| △t |
③焓变(△H)始终不变,混合气体平均相对分子质量(
. |
| M |
(3)①左端为负极,在酸性电解质中失去电子生成氮气和氢离子;
②该燃料电池的能量利用率为80%,即电池转移电子的80%=电解中转移电子,结合电子转移守恒计算.
解答:
解:(1)由①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×
得到4NH3(g)+3O2(g)=2N2(g)+6H2O(l),则△H=
,
故答案为:
;
(2)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低,则T1<T2,故答案为:<;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
v(H2)=
=
=0.1mol?L-1?min-1,
平衡时N2的转化率α(N2)=
×100%=25%,
故答案为:0.1mol?L-1?min-1;25%;
③焓变(△H)始终不变,混合气体平均相对分子质量(
)为变量、N2体积分数φ(N2)为变量,气体密度(ρ)始终不变,随反应进行,气体的物质的量减小,则
随时间增大而增大,直到达到平衡状态不变;N2体积分数逐渐减小,到达到平衡状态不变,由图可知,正确且能表明该可逆反应达到平衡状态的为BC,
故答案为:BC;
(3)①由氢离子的移动方向可知,M区为负极,发生的电极反应式为N2H4-4e-=N2↑+4H+,故答案为:N2H4-4e-=N2↑+4H+;
②用惰性电极,电解饱和KCl总的电极反应式为2Cl-+2H2O
H2↑+Cl2↑+2OH-,pH值变为13时,c(OH-)=0.1mol/L,n(OH-)=0.1mol/L×0.5L=0.05mol,
N2H4~4e-~4OH-
32g 4mol
x×80% 0.05mol,
解得x=0.5g,
故答案为:0.5.
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×
| 1 |
| 5 |
| 3△H1+2△H2 |
| 5 |
故答案为:
| 3△H1+2△H2 |
| 5 |
(2)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低,则T1<T2,故答案为:<;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
v(H2)=
| △c |
| △t |
| ||
| 10min |
平衡时N2的转化率α(N2)=
| 1 |
| 4 |
故答案为:0.1mol?L-1?min-1;25%;
③焓变(△H)始终不变,混合气体平均相对分子质量(
. |
| M |
. |
| M |
故答案为:BC;
(3)①由氢离子的移动方向可知,M区为负极,发生的电极反应式为N2H4-4e-=N2↑+4H+,故答案为:N2H4-4e-=N2↑+4H+;
②用惰性电极,电解饱和KCl总的电极反应式为2Cl-+2H2O
| ||
N2H4~4e-~4OH-
32g 4mol
x×80% 0.05mol,
解得x=0.5g,
故答案为:0.5.
点评:本题考查较综合,涉及化学平衡图象、平衡计算、盖斯定律的应用及计算、电化学原理及计算等,综合性较强,侧重化学反应原理中高频考点的考查,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知下面三个数据:7.2×10-4 mol?L-1、4.6×10-4 mol?L-1、4.9×10-10 mol?L-1分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2═HCN+NaNO2 NaCN+HF═HCN+NaF NaNO2+HF═HNO2+NaF.由此可判断下列叙述不正确的是( )
| A、碱性强弱顺序:NaF<NaNO2<NaCN |
| B、K(HNO2)=4.9×10-10 mol?L-1 |
| C、一元弱酸的强弱顺序为HF>HNO2>HCN |
| D、K(HCN)<K(HNO2)<K(HF) |
下列化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 | ||
B、S2-的结构示意图: | ||
C、中子数为20的氯原子:
| ||
D、羟基的电子式: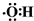 |
某原电池的电池反应为:Fe+2Fe3+═3Fe2+,与此电池反应相符的原电池是( )
| A、铜片、铁片、FeCl2溶液组成的原电池 |
| B、石墨、铁片、Fe(NO3)3溶液组成的原电池 |
| C、铁片、锌片、Fe2(SO4)3溶液组成的原电池 |
| D、银片、铁片、Fe(NO3)2溶液组成的原电池 |
由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸,再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为( )
| A、0.1 mol |
| B、大于或等于0.2 mol且小于0.3 mol |
| C、等于0.2 mol |
| D、大于0.1 mol且小于0.3 mol |
 X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:
X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:



