题目内容
为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理使钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。其过程可用下列化学方程式表示:
①3Fe NaNO2
NaNO2 5NaOH
→ 3Na2FeO2
5NaOH
→ 3Na2FeO2 H2O
H2O NH3↑
NH3↑
② Na2FeO2 NaNO2
NaNO2 H2O → Na2Fe2O4
H2O → Na2Fe2O4 NH3↑
NH3↑ NaOH
NaOH
③Na2FeO2 Na2Fe2O4
Na2Fe2O4 2H2O
2H2O Fe3O4
Fe3O4 4NaOH
4NaOH
(1)配平化学方程式②。
(2)上述反应①中还原剂为 ,被还原的是 。若有1mol Na2FeO2生成,则反应中有 mol电子转移。
(3)关于形成“发蓝”的过程,下列说法正确的是…………………………………………( )
A.该生产过程不会产生污染 B.反应③生成的四氧化三铁具有抗腐蚀作用
C.反应①②③均是氧化还原反应 D.反应①②中的氧化剂均为NaNO2
(4)当NaOH溶液浓度过大,“发蓝”的厚度会变小,其原因是: 。
(1)6,1,5,3,1,7 (1分)
(2)Fe (1分) 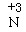 或+3价的N
(1分) 2 (1分)
或+3价的N
(1分) 2 (1分)
(3)BD (2分)
(4)反应③可逆,氢氧化钠浓度过大,平衡向逆反应方向移动 (2分)
【解析】
试题分析:
(1)由化合价升降法配平,Na2FeO2 :Fe(+2)→Na2Fe2O4 :Fe(+3) 2个Fe升高2;NaNO2:N(+3)→NH3 N(-3),N降低6 ,最小公倍数6,Na2FeO2 前填6 ;Na2Fe2O4前填3;NaNO2 和NH3前填1,其他观察法配平。
(2)1mol Na2FeO2 变成Na2Fe2O4,化合价升高2,电子转移为2mol。
(3)A、有NH3 会产生污染,错误;B、生成Fe3O4,有致密的保护层,有抗腐蚀作用 ,正确;C、③不是氧化还原反应,错误;D 、NaNO2:N(+3)→NH3 N(-3),化合价降低,做氧化剂,正确。
考点:本题以生活常识为基础,考查氧化还原反应等知识。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案 Fe3O4+4NaOH
Fe3O4+4NaOH