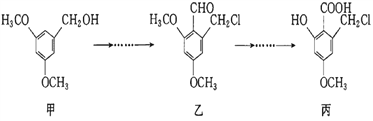
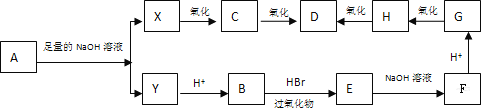
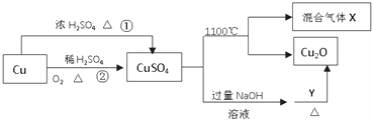
题目内容
【题目】A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示:
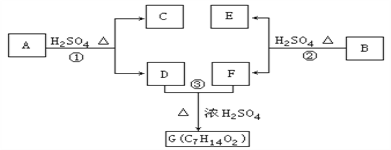
(1)化合物C的分子式是C7H8O,C遇到FeCl3溶液显示紫色,C与溴水反应生成的一溴代物只有两种,则C的结构简式为__________________;
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO3反应放出CO2,则D分子式为_____________,D具有的官能团是________________;
(3)反应①的化学方程式是_____________________________;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和F,F可能的结构简式是______________________________;
(5)E可能的结构简式是______________________________。
【答案】 ![]() C4H8O3 羧基
C4H8O3 羧基  CH3CH2CH2OH、CH3CH(OH)CH3
CH3CH2CH2OH、CH3CH(OH)CH3 
【解析】(1)C遇FeCl3溶液显紫色,说明C中有酚羟基结构;C的苯环上的一溴代物只有两种,且C为C7H8O,所以C的结构简式为![]() 。(2)D的相对分子质量比C的小20,所以D的相对分子质量为88,D能与NaHCO3反应放出CO2,则D中有—COOH,且D为直链化合物,所以D的分子式为C4H8O2,结构简式为CH3CH2CH2COOH。(3)根据上述分析,A的结构简式应为
。(2)D的相对分子质量比C的小20,所以D的相对分子质量为88,D能与NaHCO3反应放出CO2,则D中有—COOH,且D为直链化合物,所以D的分子式为C4H8O2,结构简式为CH3CH2CH2COOH。(3)根据上述分析,A的结构简式应为 。(4)由于D和F产生G;且G的分子式为C7H14O2,所以F分子式为C3H8O,结构简式可能为:CH3CH2CH2OH,
。(4)由于D和F产生G;且G的分子式为C7H14O2,所以F分子式为C3H8O,结构简式可能为:CH3CH2CH2OH, 。(5)由于B为芳香化合物,且与A互为同分异构体,所以E的分子式为C8H8O2,E可能的结构简式便可推出。
。(5)由于B为芳香化合物,且与A互为同分异构体,所以E的分子式为C8H8O2,E可能的结构简式便可推出。

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料。工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)制备,其制备过程如下:
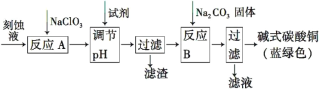
查阅资料知,通过调节溶液的酸碱性可使Cu2+,Fe2+,Fe3+生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀pH | 4.7 | 7.5 | 1.4 |
沉淀完全pH | 6.7 | 14 | 3.7 |
(1)氯酸钠的作用是______________________________________。
(2)调节反应A所得溶液的pH范围为_______________________,
可以选择的试剂是______(填序号)。
a.氨水 b.硫酸铜 c.氢氧化铜 d.碱式碳酸铜
(3)反应B的温度要控制在60℃左右,且保持恒温,可采用的加热方法是________;若温度过高,所得蓝绿色沉淀中会有黑色固体出现,黑色固体可能是________。
(4)已知滤液中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式:______________________________________________。
(5)过滤得到的产品洗涤时,如何判断产品已经洗净____________________。