��Ŀ����
 I���ɻ�β���е�NO���ƻ������㣮���ô�
I���ɻ�β���е�NO���ƻ������㣮���ô�������ʹβ���е�NO��CO������Ӧ2NO+2CO?2CO2+N2����H��0����֪��������ȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�������Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ���
| ʵ���� | T���棩 | NO��ʼŨ�ȣ�mol/L�� | CO��ʼŨ�ȣ�mol/L�� | �����ıȱ������m2/g�� |
| �� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
| �� | 1.20��10-3 | 124 | ||
| �� | 350 | 5.80��10-3 |
��2���������ϱ߸���������ͼ�У������ϱ��е�����ʵ�������»��������NOŨ����ʱ��仯����������ͼ���������������ߵ�ʵ���ţ�
II��������ȼ������ʱ�����ĸ��»�����N2��O2�ķ�Ӧ��N2��g��+O2��g��?2NO��g���ǵ�������β���к���NO��ԭ��֮һ��
200��ʱ�����ݻ�Ϊ2L���ܱ������г���10molN2��5mol O2���ﵽƽ���NO�����ʵ���Ϊ2mol����÷�Ӧ��ƽ�ⳣ��K=
���㣺̽��Ӱ�컯ѧ��Ӧ���ʵ�����,���ʵ�����Ũ����ʱ��ı仯����,��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��,��ѧ��Ӧ����ר��
������I������ʵ��Ŀ����֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ���Ӧ��֤Ũ����ͬ��Ȼ����ͬ�¶�ʱ�Ƚϴ����ȱ��������ͬ�����ȱ����ʱ�Ƚ��¶ȣ�Ȼ������Ӱ�컯ѧ��Ӧ���ʼ���ѧƽ�������������ͼ��
II��K=
���¶Ȳ���ƽ�ⳣ�����䣬����ƽ�ⳣ�����㵪����ƽ�����ʵ�����
II��K=
| c2(NO) |
| C(N2)��C(O2) |
���
�⣺I����1�������ȱ������ͬ����Ӧ�����¶���ͬ������Ũ��Ӧ������ͬ����֤�����ȱ���������ʵ�Ӱ�죻
��ȱ������ͬ���¶Ȳ�ͬ��������Ũ��Ӧ������ͬ����֤��Ӧ�¶ȶ����ʵ�Ӱ�죻��
�ʴ�Ϊ��280��5.80��10-3��1.20��10-3��124��
������¶���ͬ��������ƽ���ƶ���Ӱ�죬��ƽ�ⲻ�ƶ�����������ʴ�����ȴﵽ��ѧƽ�⣬���ƽ��ʱNO��Ũ����ͬ��������¶ȸߣ���Ӧ���������ƽ�����ƣ����ﵽ��ѧƽ��ʱc��NO�����ʴ�Ϊ�� ��
��
II���ﵽƽ���NO�����ʵ���Ϊ2mol����c��NO��=
=1mol/L��c��N2��=
=4.5mol/L��c��O2��=
=2mol/L��K=
=
��
��ƽ��ʱ���������ʵ���x����Ͷ������������ʵ���Ϊy��
N2��g��+O2��g��?2NO��g��
��ʼ 1mol ymol 0
��Ӧ��1-x��mol ��1-x��mol 2��1-x��mol
ƽ��xmol ��y-1+x��mol 2��1-x��mol
ƽ��Ũ��c��NO��=
mol/L��c��N2��=
mol/L��c��O2��=
mol/L��K=
=
�٣�
��y-1+x��mol=2��1-x��mol �ڣ������٢ڵ�
�����Ե�����ƽ��Ũ��Ϊ
mol��
�ʴ�Ϊ��
��
��
��ȱ������ͬ���¶Ȳ�ͬ��������Ũ��Ӧ������ͬ����֤��Ӧ�¶ȶ����ʵ�Ӱ�죻��
�ʴ�Ϊ��280��5.80��10-3��1.20��10-3��124��
������¶���ͬ��������ƽ���ƶ���Ӱ�죬��ƽ�ⲻ�ƶ�����������ʴ�����ȴﵽ��ѧƽ�⣬���ƽ��ʱNO��Ũ����ͬ��������¶ȸߣ���Ӧ���������ƽ�����ƣ����ﵽ��ѧƽ��ʱc��NO�����ʴ�Ϊ��
 ��
��II���ﵽƽ���NO�����ʵ���Ϊ2mol����c��NO��=
| 2mol |
| 2L |
| (10-1)mol |
| 2L |
| (5-1)mol |
| 2L |
| 1��1 |
| 4.5��2 |
| 1 |
| 9 |
��ƽ��ʱ���������ʵ���x����Ͷ������������ʵ���Ϊy��
N2��g��+O2��g��?2NO��g��
��ʼ 1mol ymol 0
��Ӧ��1-x��mol ��1-x��mol 2��1-x��mol
ƽ��xmol ��y-1+x��mol 2��1-x��mol
ƽ��Ũ��c��NO��=
| 1-x |
| 2 |
| x |
| 2 |
| y-1+x |
| 2 |
| ||||
|
| 1 |
| 9 |
��y-1+x��mol=2��1-x��mol �ڣ������٢ڵ�
|
| 9 |
| 11 |
�ʴ�Ϊ��
| 1 |
| 9 |
| 9 |
| 11 |
������ע�ؿ�����ѧ���Ի�ѧʵ������˼·������������¿γ̱仯��ͬʱ��ע���˶Ը߿��ȵ�Ŀ��飬�ǽϺõ�һ���ۺ��⣬ע��ƽ�ⳣ�����¶ȵĹ�ϵ��Ϊ�״��㣮

��ϰ��ϵ�д�
�����Ŀ
�ѣ�Ti������Ϊ���������������Ti0����ȡTi����Ҫ��Ӧ��
��Ti02+2Cl2+2C
TiCl4+2CO
��TICl4+2Mg
2MgCl2+Ti
����˵������ȷ���ǣ�������
��Ti02+2Cl2+2C
| ||
��TICl4+2Mg
| ||
����˵������ȷ���ǣ�������
| A����Ӧ�٢ڶ���������ԭ��Ӧ |
| B����Ӧ�����û���Ӧ |
| C����Ӧ����Ti02���������� |
| D����Ӧ����ÿ����1mol Tiת��4 mol���� |
�������ʵ���;�У�Ӧ�õ����ʵ������Ե��ǣ�������
| A����������ˮ |
| B��Cl0��������ˮ |
| C�������ȥ���� |
| D��С�մ�����θ����� |

 �������ϰ�װ��ת������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯������Ӧ�����������ʣ���������β����Ⱦ��
�������ϰ�װ��ת������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯������Ӧ�����������ʣ���������β����Ⱦ��
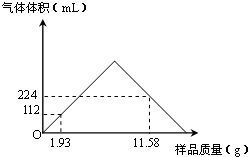 ������������ʵ���Һ�ҵ�����ж��й㷺����;��
������������ʵ���Һ�ҵ�����ж��й㷺����;��