题目内容
8.一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+S(l)△H<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )| A. | 平衡前,随着反应的进行,容器内压强始终不变 | |
| B. | 平衡时,其他条件不变,分离出硫,正反应速率加快 | |
| C. | 平衡时,其他条件不变,升高温度可提高SO2的转化率 | |
| D. | 其他条件不变,缩小体积,平衡右移,SO2浓度增大 |
分析 该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,容器内气体的压强在不断减小,升高温度平衡向逆反应方向移动,以此解答该题.
解答 解:A.该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,随着反应的进行,气体的物质的量逐渐减小,则容器的压强在逐渐减小,故A错误;
B.硫是液体,分离出硫,气体反应物和生成物浓度都不变,所以不影响反应速率,故B错误;
C.该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,抑制了二氧化硫的转化,所以二氧化硫的转化率降低,故C错误;
D.其他条件不变,缩小体积,压强增大,平衡正向移动,但因体积减小,则SO2浓度增大,故D正确.
故选D.
点评 本题考查化学平衡影响因素,为高频考点,侧重考查学生分析判断能力,明确温度、压强、浓度对化学平衡影响原理是解本题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.既能发生加成反应、酯化反应,又能发生氧化反应的有机物是( )
| A. | CH2OHCHOHCH2OH | B. | CH2=CH-CH2OH | C. | CH2=CH-COOCH3 | D. | CH2=CH-COOH |
20.下列含有共价键的离子化合物是( )
| A. | CO2 | B. | NaOH | C. | CaF2 | D. | 金刚石 |
17.如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )


| A. | ZM2分子中各原子的最外层均满足8电子稳定结构 | |
| B. | 离子半径:M->Z2->Y- | |
| C. | 电负性:Y>Z>M | |
| D. | Z元素基态原子最外层电子排布图为: |
2.含有一个双键的烯烃,加氢后产物的结构简式为  ,此烯烃可能的结构有( )
,此烯烃可能的结构有( )
 ,此烯烃可能的结构有( )
,此烯烃可能的结构有( )| A. | 4种 | B. | 6种 | C. | 8种 | D. | 10种 |
 .
. 和
和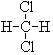 ; ⑦CH3 (CH2) 3CH3和
; ⑦CH3 (CH2) 3CH3和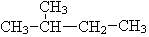
 根据有机物在化学反应中断键的位置,可以准确分析产物结构并判断反应类型.有机物A中只含有C、H、O三种元素,它的球棍模型如下:
根据有机物在化学反应中断键的位置,可以准确分析产物结构并判断反应类型.有机物A中只含有C、H、O三种元素,它的球棍模型如下: .
.