题目内容
已知铅蓄电池放电时的电极反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
若用此电池(惰性电极)电解饱和食盐水,当阴、阳两极收集到的气体总体积为1.68L(标准状况)时,该蓄电池内消耗H2SO4______。
答案:
解析:
解析:
电解的总反应式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O,而电解食盐水共收集到气体0.075mol气体,电子转移数为0.15mol,所以消耗的硫酸的物质的量为0.3mol。
|

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
 我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列有关说法正确的是( )
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列有关说法正确的是( )| A、图中涉及的能量转化方式只有3种 | ||
B、蓄电池供电时,负极的电极反应为:Pb+SO
| ||
| C、储能时若充电时间过长,阳极流向阴极的气体可能是H2 | ||
| D、该发电工艺不可实现零排放 |
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列有关说法正确的是( )
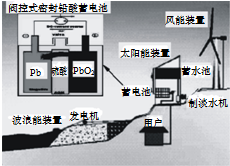

| A、图中涉及的能量转化方式只有3种 | B、蓄电池供电时,负极的电极反应为:Pb+SO42--2e-=PbSO4 | C、储能时若充电时间过长,阳极流向阴极的气体可能是H2 | D、该发电工艺可实现零排放 |
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:
Pb+PbO2+2H2SO4 = 2PbSO4+2H2O,下列有关说法正确的是
| A.图中涉及的能量转化方式只有3种 |
| B.该发电工艺可实现零排放 |
| C.蓄电池供电时,负极的电极反应为:Pb-2e-=Pb2+ |
| D.储能时若充电时间过长,阳极流向阴极的气体可能是H2 |
实验室用铅蓄电池作电源电解水,已知铅蓄电池放电时的电极反应如下:
负极:Pb + SO42――2e―="=" PbSO4
正极:PbO2 + 4H+ + SO42―+2e― ="=" PbSO4+ 2H2O
若制得0.1mol 的H2,此时电池内消耗的硫酸的物质的量至少是
| A.0.025 mol | B.0.50 mol | C.0.10 mol | D.0.20 mol |
