题目内容
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各
元素中电负性最大。请回答下列问题:
(1) X、Y的元素符号依次为 、 ;
(2) XZ2与YZ2分子的立体结构分别是V形(1分)和直线形(1分),相同条件下两者在水中的溶解度较大的是 (1分)(写分子式)’理由是因为 (2分);
(3) Q的元素符号是 (1分),它属于 周期,它的核外电子排布式为 (1分),在形成化合物时它的最髙化合价为 ;
(4) 用氢键表示式写出??的氢化物溶液中存在的所有氢键 (4 分)。
(1) S (1分)、C (1分);
(2) V形(1分)和直线形(1分), SQ2 (1分)(写分子式)’,SO2在H2O中的溶解度较大(2分);
(3) Cr (1分),它属于第四 (1分)周期,它的核外电子排布式为![]() 1分),在形成化合物时它的最髙化合价为+6 (1分);
1分),在形成化合物时它的最髙化合价为+6 (1分);
(4) ![]() (4 分)。
(4 分)。
解析:
略

练习册系列答案
相关题目
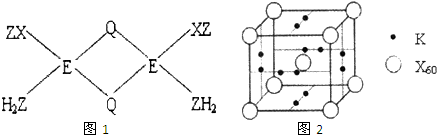 已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题:
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题: