题目内容
下列粒子中可能存在配位键的是( )
分析:判断分子中能否有提供孤电子对和空轨道的粒子,以此来解答.
解答:解:A.CO2中C原子和O通过共用电子对形成共价键,没有配位键,故A错误;
B.H3O+中O提供孤电子对,H+提供空轨道,二者都能形成配位键,故B正确;
C.CH4中C原子和H通过共用电子对形成共价键,没有配位键,故C错误;
D.H2SO4的结构是以硫为中心,含有两个硫氧双键和两个硫氧单键,两个单键氧又各与一个氢结合,没有配位键,故D错误;
故选:B.
B.H3O+中O提供孤电子对,H+提供空轨道,二者都能形成配位键,故B正确;
C.CH4中C原子和H通过共用电子对形成共价键,没有配位键,故C错误;
D.H2SO4的结构是以硫为中心,含有两个硫氧双键和两个硫氧单键,两个单键氧又各与一个氢结合,没有配位键,故D错误;
故选:B.
点评:本题主要考查配位键的形成条件,掌握形成条件是解题的关键,难度中等.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
(10分)配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
| A.CO2 | B.H3O+ | C.CH4 | D.NH4+ |
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲:
 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)乙:HOOH
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:_____________________________________________________________。
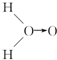 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
 、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验: (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)