题目内容
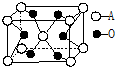 过渡元素的化合物是高温超导物质研究的热点.某过渡元素A与氧形成的化合物叫金红石,其晶体的最小结构单元如图.则下面有关金红石的说法正确的是( )
过渡元素的化合物是高温超导物质研究的热点.某过渡元素A与氧形成的化合物叫金红石,其晶体的最小结构单元如图.则下面有关金红石的说法正确的是( )分析:金属元素和非金属氧元素形成的化合物可能是离子化合物,根据均摊法计算氧化物中A与氧原子的个数比,从而确定其化学式.
解答:解:A、过渡元素都是金属元素,所以某过渡元素A是金属元素,活泼金属和活泼非金属元素之间易存在离子键,金属元素和非金属元素之间可能存在共价键,所以金红石含有的化学键可能是共价键,而非一定是共价键,故A错误.
B、过渡元素都是金属元素,所以某过渡元素A是金属元素,活泼金属和活泼非金属元素之间易存在离子键,金属元素和非金属元素之间可能存在共价键,所以金红石含有的化学键可能是离子键,故B正确.
C、该晶胞中含有的O原子个数为2+
×4=4,A原子个数=1+
×8=1+1=2,所以它的化学式为AO2,故C正确.
D、该晶胞中含有的O原子个数为2+
×4=4,A原子个数=1+
×8=1+1=2,所以它的化学式为AO2,故D错误.
故选BC.
B、过渡元素都是金属元素,所以某过渡元素A是金属元素,活泼金属和活泼非金属元素之间易存在离子键,金属元素和非金属元素之间可能存在共价键,所以金红石含有的化学键可能是离子键,故B正确.
C、该晶胞中含有的O原子个数为2+
| 1 |
| 2 |
| 1 |
| 8 |
D、该晶胞中含有的O原子个数为2+
| 1 |
| 2 |
| 1 |
| 8 |
故选BC.
点评:本题考查了晶胞的计算,难度不大,注意金属元素和非金属元素形成的化合物不一定是离子化合物,如氯化铝是共价化合物.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目