题目内容
【题目】有A、B、C、D四种元素,A元素的原子得2个电子、B元素的原子失去1个电子后所形成的微粒均与氩原子有相同的核外电子数。C元素的原子只有1个电子,A、D两元素原子核外电子总数比B元素原子质子数多9个。
(1)A的元素名称是_______,B的元素符号是______。
(2)D原子的原子结构示意图为____________,B+的离子结构示意图__________。
【答案】硫 K ![]()
![]()
【解析】
由题意可知,A元素的原子得到2个电子、B元素的原子失去1个电子后,所形成的微粒均与氩原子具有相同的核外电子数,则A为硫元素,B为钾元素;C元素的原子只有1个电子,则C为氢元素;A、D两元素原子核外电子总数比B元素原子质子数多9个,则D是镁元素。
(1)由以上分析,可得出A的元素名称和B的元素符号。
(2)D为镁,其原子核外电子数为12,呈2、8、2分布,由此可写出其原子结构示意图,B+的符号为K+,离子核外有18个电子,呈2、8、8分布,由此可写出其离子结构示意图。
(1)由以上分析,可确定A为硫,B为钾,则A的元素名称是硫,B的元素符号是K。答案为:硫;K;
(2)D为镁,其原子核外电子数为12,呈2、8、2分布,则其原子结构示意图为![]() ,B+的符号为K+,离子核外有18个电子,呈2、8、8分布,其离子结构示意图为
,B+的符号为K+,离子核外有18个电子,呈2、8、8分布,其离子结构示意图为![]() 。
。
答案为:![]() ;
;![]() 。
。

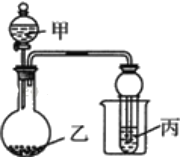
【题目】一定条件下,向容器中同时通入甲烷、氧气和水蒸气三种气体,发生的化学反应有:
反应过程 | 化学方程式 | 焓变
| 活化能
|
甲烷氧化 |
|
|
|
|
|
| |
蒸汽重整 |
|
|
|
|
|
|
(1)已知:![]() ,则
,则![]() 燃烧热
燃烧热![]() _____。
_____。
(2)在初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率,原因可能是______。
(3)恒温恒压体系(温度为![]() ,压强为
,压强为![]() ),反应
),反应![]() 达到平衡时,各气体的物质的量均为
达到平衡时,各气体的物质的量均为![]() ,用某气体组分
,用某气体组分![]() 的平衡分压(分压=总压×物质的量分数)代替物质的量浓度
的平衡分压(分压=总压×物质的量分数)代替物质的量浓度![]() 也可表示平衡常数(记作
也可表示平衡常数(记作![]() )。则:
)。则:
①平衡常数![]() ___。
___。
②再向容器中瞬时同时充入![]() 、
、![]() 、
、![]() 、
、![]() ,此时
,此时![]() (正)____
(正)____![]() (逆)(填“>”“<”或“=”)
(逆)(填“>”“<”或“=”)
③恒温恒容条件下,将![]() 、
、![]() 、
、![]() 、
、![]() 按照体积比
按照体积比![]() 投料,能判断反应
投料,能判断反应![]() 达到平衡状态的是____。
达到平衡状态的是____。
A 密度保持不变 B ![]() 体积分数保持不变
体积分数保持不变
C 平均摩尔质量保持不变 D ![]() 和
和![]() 的比保持不变
的比保持不变
E ![]() 断裂的同时,有
断裂的同时,有![]() 断裂
断裂
(4)向绝热恒容密闭容器中通入![]() 和
和![]() 使反应
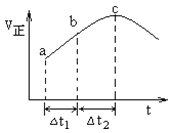
使反应![]() 达到平衡,正反应速率随时间变化的示意图如图所示。图中
达到平衡,正反应速率随时间变化的示意图如图所示。图中![]() 点反应是否达到平衡,说明理由_____。
点反应是否达到平衡,说明理由_____。
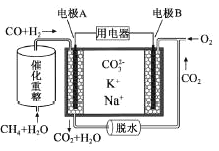
(5)利用重整反应![]() ,设计一种熔融碳酸盐燃料电池,原理示意图,电极
,设计一种熔融碳酸盐燃料电池,原理示意图,电极![]() 上发生的电极反应为______。
上发生的电极反应为______。