题目内容
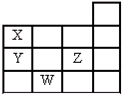 如图表示元素周期表中1~4周期的一部分,关于元素X、Y、Z、W的叙述错误的是( )
如图表示元素周期表中1~4周期的一部分,关于元素X、Y、Z、W的叙述错误的是( )| A、X、Y的最高价氧化物的水化物酸性为Y<X | B、Y、Z的气态氢化物的稳定性为Y<Z | C、Z有5种不同运动状态的电子 | D、W的原子序数比Y大19 |
分析:由元素在周期表中的位置可知,X为N元素,Y为P元素,Z为Cl元素,W为Se元素,
A、同主族自上而下非金属性减弱,非金属性越强,最高价氧化物的水化物酸性越强;
B、同周期自左而右非金属性增强,非金属性越强,氢化物越稳定;
C、原子中核外电子没有运动状态相同的电子,核外有几种电子具有几种不同运动状态的电子;
D、W为Se元素,原子序数为34.
A、同主族自上而下非金属性减弱,非金属性越强,最高价氧化物的水化物酸性越强;
B、同周期自左而右非金属性增强,非金属性越强,氢化物越稳定;
C、原子中核外电子没有运动状态相同的电子,核外有几种电子具有几种不同运动状态的电子;
D、W为Se元素,原子序数为34.
解答:解:由元素在周期表中的位置可知,X为N元素,Y为P元素,Z为Cl元素,W为Se元素,
A、同主族自上而下非金属性减弱,故非金属性N>P,故最高价氧化物的水化物酸性:N>P,故A正确;
B、同周期自左而右非金属性增强,故非金属性P<Cl,故氢化物稳定性:PH3<HCl,故B正确;
C、Z为Cl元素,原子中核外由17个电子,高于核外有17种不同运动状态的电子,故C错误;
D、W为Se元素,原子序数为34,故D正确;
故选C.
A、同主族自上而下非金属性减弱,故非金属性N>P,故最高价氧化物的水化物酸性:N>P,故A正确;
B、同周期自左而右非金属性增强,故非金属性P<Cl,故氢化物稳定性:PH3<HCl,故B正确;
C、Z为Cl元素,原子中核外由17个电子,高于核外有17种不同运动状态的电子,故C错误;
D、W为Se元素,原子序数为34,故D正确;
故选C.
点评:本题考查元素周期表、元素周期律、核外电子运动等,难度不大,注意整体把握元素周期表的结构,注意C选项中原子中核外电子没有运动状态相同的电子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
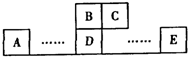 如图为元素周期表中的一部分,A、B、C、D、E均为短周期主族元素,B元素原子的最外层有4个电子,E原子最外层电子数与C的原子序数相等.回答下列问题:
如图为元素周期表中的一部分,A、B、C、D、E均为短周期主族元素,B元素原子的最外层有4个电子,E原子最外层电子数与C的原子序数相等.回答下列问题: 如图是元素周期表中1~20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
如图是元素周期表中1~20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
 如图是元素周期表中1~20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
如图是元素周期表中1~20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知: