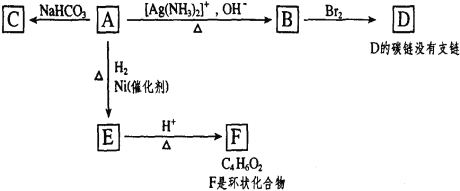
题目内容
【题目】在25℃时,碳酸钙在水中的沉淀溶解平衡曲线如图所示,已知25℃时硫酸钙的Ksp=9.1×10-6。
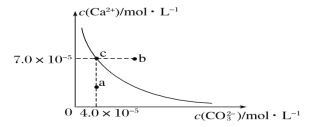
(1)通过蒸发,可使稀溶液由_______点变化到_______点。
(2)在25℃时,反应CaSO4(s)+CO32- (aq)CaCO3(s)+SO42-(aq)的平衡常数K_______
【答案】a b 3250
【解析】
(1)CaCO3在水中的沉淀溶解平衡为CaCO3(s)![]() Ca2+(aq)+CO32-(aq),图象中位于曲线上的c点为饱和溶液,处于溶解平衡状态,a点处离子浓度小于饱和溶液浓度为不饱和溶液,b点为过饱和溶液,根据平衡状态的移动原理解答该题;
Ca2+(aq)+CO32-(aq),图象中位于曲线上的c点为饱和溶液,处于溶解平衡状态,a点处离子浓度小于饱和溶液浓度为不饱和溶液,b点为过饱和溶液,根据平衡状态的移动原理解答该题;
(2)根据K=  =
=  计算。
计算。
(1)由分析可知,CaCO3在水中的沉淀溶解平衡为CaCO3(s)![]() Ca2+(aq)+CO32-(aq),图象中位于曲线上的c点为饱和溶液,处于溶解平衡状态,a点处离子浓度小于饱和溶液浓度为不饱和溶液,b点为过饱和溶液。通过蒸发,溶液体积减小,钙离子和碳酸根离子的浓度均增大,能使溶液由a点变化到b点;
Ca2+(aq)+CO32-(aq),图象中位于曲线上的c点为饱和溶液,处于溶解平衡状态,a点处离子浓度小于饱和溶液浓度为不饱和溶液,b点为过饱和溶液。通过蒸发,溶液体积减小,钙离子和碳酸根离子的浓度均增大,能使溶液由a点变化到b点;
(2)在25℃时,反应CaSO4(s)+CO32-(aq) CaCO3(s)+SO42-(aq)的平衡常数K= =
=  =
= =
=![]() =3250。
=3250。

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2 mol的A和0.8 mol的B,反应初始4 s内A的平均反应速率υ(A)=0.005 mol/(L·s)。下列说法正确的是
A. 4 s时c(B)为0.38 mol/L
B. 830℃达平衡时,A的转化率为20%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数为0.4
A(g)+B(g)的平衡常数为0.4
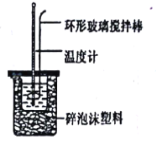
【题目】实验室用50mL0.50mol/L盐酸、50mL0.55mol/LNaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.3 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 26.9 |
完成下列问题:
(1)根据上表中所测数据,该实验中和热△H=___。(不必计算和化简,代入数据即可)[盐酸和NaOH溶液的密度按1g/cm3计算,反应后混合溶液的比热容(c)按4.18J/(g·℃)计算]。
(2)在该实验过程中,该同学需要测定的实验数据有___(填序号)。
A.盐酸的浓度 B.盐酸的温度
C.氢氧化钠溶液的浓度 D.氢氧化钠溶液的温度
E.水的比热容 F.反应后混合溶液的终止温度