题目内容
A、B、C、D、E五种短周期元素,原子序数依次递增,A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,而E在同周期元素中原子半径最小。A、C、D三种元素可形成化合物甲,B、C、D三种元素可形成化合物乙,甲和乙均为中学化学常见物质。请回答:
(1)甲的电子式为 ,其中所含化学键类型为 。
(2)A的单质与C的单质在碱性条件下构成燃料电池,其正极反应式为 ;负极反应式 为。
(3)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH—的物质的量浓度c(OH—)甲:c(OH—)乙= .
(4)A与C、D与C可形成化合物A2C、A2C2、D2C、D2C2,说出的一种用途 ;
写出A2C2与E的单质反应的化学方程式 。
(5)浓氨水与固体甲混合,可用于快速制取少量氨气,其原因是
(请用必要的方程式和简要的文字加以说明)。
(1)Na+[:O:H ]-,(1分)离子键和极性共阶键(1分)
(2))O2+2H2O+4e-=40H-(1分);2H2-4e-+4OH-=4H2O(1分)
(3)10-4:1(2分)
(4))潜水艇的生氧剂(防毒面具的生氧剂或其他合理答案)(1分);H2O2+Cl2 = 2HCl+O2(2分)。
(5)在氨水中有下列平衡:NH3+H2O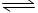 NH3·H2O
NH3·H2O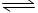 NH
NH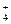 +OH-,NaOH固体溶于水放热,使得氨气的溶解度减小,同时增大了溶液中的c(OH-),促使化学平衡逆向移动(2分)。
+OH-,NaOH固体溶于水放热,使得氨气的溶解度减小,同时增大了溶液中的c(OH-),促使化学平衡逆向移动(2分)。
解析由A原子形成的阳离子是一个质子,则A为氢元素;由B原子的最外层电子数是次外层的2倍,则B为碳元素;由C原子的最外层电子数与B原子的核外电子总数相等,则C的核外电子排布可能是两电子层2、6,或三电子层2、8、6,即为氧元素或硫元素,而由D在同周期元素中原子半径最大,且D的原子序数大于B、C,则D只能是Na元素,C只能是氧元素;E为氯元素。

 初中学业考试导与练系列答案
初中学业考试导与练系列答案





 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )