题目内容
3.标准状况下,将 336mL某气态烷烃完全燃烧,把产生的气体全部通过盛浓硫酸的洗气瓶,洗气瓶增重 1.35g,则该烷烃为( )| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C4H10 |
分析 烷烃的物质的量为$\frac{0.336L}{22.4L/mol}$=0.015mol,把产生的气体全部通过盛浓硫酸的洗气瓶,洗气瓶增重 1.35g,为水的质量,且水的物质的量为$\frac{1.35g}{18g/mol}$=0.075mol,以此可确定烷烃的H原子数,结合烷烃的通式CnH2n+2计算.
解答 解:烷烃的物质的量为$\frac{0.336L}{22.4L/mol}$=0.015mol,把产生的气体全部通过盛浓硫酸的洗气瓶,洗气瓶增重 1.35g,为水的质量,且水的物质的量为$\frac{1.35g}{18g/mol}$=0.075mol,则n(H)=0.15mol,所以1mol烷烃含有的H原子数为$\frac{0.15mol}{0.015mol}$=10,烷烃的通式CnH2n+2,则分子式为C4H10,
故选D.
点评 本题考查了烷烃分子式的确定,题目难度不大,根据相同条件下气体体积比等于物质的量之比计算出碳原子是解题关键,注意明确质量守恒在确定有机物分子式中的应用方法.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
16.下列化学用语表述正确的是( )
| A. | 甲烷的球棍模型: | B. | CS2的电子式为: | ||
| C. | HClO的结构式为:H-Cl-O | D. | NH4Cl的电子式: |
17.钠与水反应:2Na+2H2O═2NaOH+H2↑,在该反应中( )
| A. | H2O作还原剂 | B. | H2O作氧化剂 | ||
| C. | Na元素化合价降低 | D. | Na元素化合价升高 |
18.下列物质的分类结果全部正确的是( )
| A. | SiO2酸性氧化物 Na2O碱性氧化物 A12O3两性氧化物 | |
| B. | 水玻璃-混合物 冰水混合物-纯净物 HT-单质 | |
| C. | 火碱-碱 石炭酸-羧酸 小苏打-酸式盐 | |
| D. | 王水-强电解质 硫酸钡-强电解质 醋酸-弱电解质 |
15.下列对物质用途的描述中,错误的是( )
| A. | 与Mg、Al比较,镁铝合金的强度和硬度均较大,常用作航天器的材料 | |
| B. | Cl2、SO2、NaClO均可用于漂白某些物质 | |
| C. | 浓硫酸具有吸水性,可用于干燥HCl、H2S、O2 | |
| D. | 碳酸钠可用于制皂和制玻璃 |
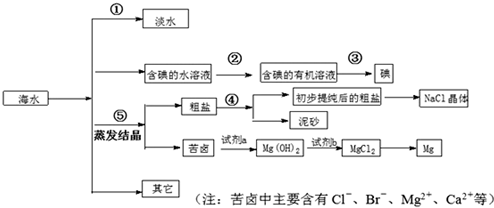
 2AB3(g) △H<0 ,则下列图像不正确的是
2AB3(g) △H<0 ,则下列图像不正确的是