题目内容
【题目】若向25mLNaOH溶液中逐滴加入0.2mol/LCH3COOH溶液过程中溶液pH的变化曲线如图所示。

(1)该NaOH溶液的物质的量浓度为_________________。
(2)a____12.5mL(填“>”,“<”或“=”),若由体积相等的氢氧化钠和醋酸溶液混合而且恰好呈中性
(3)在D点溶液中各离子浓度由大到小顺序为_____________________ .
【答案】 0.1mol·L-1 > c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
【解析】(1)由图像可知:NaOH溶液的pH=13,c(H+)=10-13,c(OH-)=10-1 mol·L-1= c(NaOH);正确答案:0.1mol·L-1。
(2)25mL、0.1mol·L-1 NaOH溶液与12.5mL、0.2mol/LCH3COOH溶液恰好完全反应生成醋酸钠溶液,溶液显碱性;若要呈中性,醋酸就得稍过量,所以a>12.5ml;正确答案:>;
(3)25mL、0.1mol·L-1 NaOH溶液与25mL、0.2mol/LCH3COOH溶液完全反应,混合液为醋酸钠和醋酸(1:1),溶液显酸性;醋酸的电离过程大于醋酸钠的水解过程,溶液中离子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(OH-);正确答案:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。查阅资料知:
①Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
②向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3。
③BaSO3难溶于水,可溶于稀HCl。
实验装置如图所示(省略夹持装置)
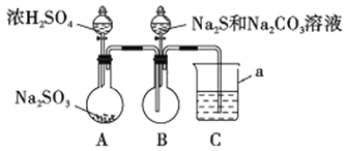
(1)仪器a的名称是_________;C中的试剂可以是______ (选填下列字母编号)。
A.稀H2SO4 B.酸性KMnO4溶液 C.饱和NaHSO3溶液 D.NaOH溶液
(2)此实验装置设计有缺陷,其改进方法是_________________________。
(3)写出B中反应的离子方程式_________________________________________。
(4)A、B中反应完后,在拆装置前,应将其中污染空气的有毒气体除去,采用的方法和具体操作是________________________________________。
(5)该法所得产品中常含有少量Na2SO3和Na2SO4。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,加足量BaCl2溶液,有白色沉淀生成,_______________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(6)测定产品纯度:准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol/L碘的标准溶液滴定。(反应原理为:2S2O32-+I2=S4O62-+2I-)
①滴定至终点时,溶液颜色的变化是_______________________。
②滴定记录数据如下表:
滴定前读数/mL | 滴定后读数/mL | |
第一次 | 0.10 | 16.12 |
第二次 | 1.10 | 17.08 |
第三次 | 1.45 | 19.45 |
第四次 | 0.00 | 16.00 |
③产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。



