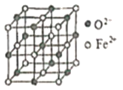
��Ŀ����
����Ŀ������������⣺
(1)10Be��9Be______________��
a����ͬһ��ԭ�ӡ�������b��������ͬ��������
c��������ͬ�Ļ�ѧ���� d��������ͬ�ĺ�������Ų�
(2)�������������ʣ�
��![]() O��
O��![]() O��
O��![]() O����H2O��D2O����ʯī�����ʯ ��H2��D2��T2����H��D��T����
O����H2O��D2O����ʯī�����ʯ ��H2��D2��T2����H��D��T����![]() K��
K��![]() Ca��
Ca��![]() Ar���ش��������⣺
Ar���ش��������⣺
a����Ϊͬλ�ص���______________��
b����Ϊͬ�����������______________��
c���ɢٺ͢��е����ܽ�ϳ�ˮ���ɵ�ˮ���ӵ�����Ϊ__________�֣��ɵ���Է���������ͬ��ˮ��������Ϊ__________�֣���Է�������������____________(д��ѧʽ)��
(3)![]() H2
H2![]() O��Ħ������Ϊ____________����ͬ������
O��Ħ������Ϊ____________����ͬ������![]() H2
H2![]() O��
O��![]() H2
H2![]() O����������֮��Ϊ______��������֮��Ϊ__________��
O����������֮��Ϊ______��������֮��Ϊ__________��
(4)�����ͬ������![]() H2
H2![]() O��
O��![]() H2
H2![]() Oʱ������������ͬ��ͬѹ�����֮��Ϊ__________������֮��Ϊ__________��
Oʱ������������ͬ��ͬѹ�����֮��Ϊ__________������֮��Ϊ__________��
���𰸡�cd �٢� �� 18 7 TO 20 g��mol��1 11��10 11��12 10��9 5��9
��������
��1��10Be��9Be��Ϊͬλ�أ����ǵ���������ͬ������������������ͬ������ͬһ��ԭ�ӣ��������Ƕ���BeԪ�ص�ԭ�ӣ���ѧ������ͬ��������ͬ�ĺ�������Ų�����ѡcd��
��2����![]() O��
O��![]() O��
O��![]() O������ԭ������������8����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
O������ԭ������������8����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
��H2O��D2O�����Dz���ԭ�ӣ�Ҳ���ǵ��ʣ�����ͬλ�ػ�ͬ����������о����룻
��ʯī�����ʯ����̼Ԫ�صĵ��ʣ���Ϊͬ�������壻
��H2��D2��T2�ֱ���![]() ��
��![]() ��
��![]() �γɵ��������ʣ����Dz���ԭ�ӣ�ȴ��ͬһ�����ʣ��������Dz���ͬλ�ػ�ͬ����������о����룻
�γɵ��������ʣ����Dz���ԭ�ӣ�ȴ��ͬһ�����ʣ��������Dz���ͬλ�ػ�ͬ����������о����룻
��H��D��T�ֱ���![]() ��
��![]() ��
��![]() �����ǵ�����������1����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
�����ǵ�����������1����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
��![]() K��
K��![]() Ca��
Ca��![]() Ar�����ǵ���������ͬ���ʱ˴˲���ͬλ�أ�
Ar�����ǵ���������ͬ���ʱ˴˲���ͬλ�أ�
��a����Ϊͬλ�ص��Ǣ٢ݣ�b����Ϊͬ����������Ǣۣ�
c���ɢ٣�![]() O��
O��![]() O��
O��![]() O���͢ݣ�H��D��T���е����ܽ�ϳ�ˮ������ˮ��������������ԭ�Ӻ�һ����ԭ�ӣ�����������ԭ�ӿ����Dz�ͬ����ģ�����ԭ�ӵġ����䡱��6�֣��ʿ��γ�ˮ���ӵ�����Ϊ18��=6��3���֣��ɵ���Է���������ͬ��ˮ��������Ϊ7�֣���Է��������ֱ���18��H216O����19��HD16O��H217O����20��D216O��HT16O��HD17O��H218O����21��DT16O��D217O��HT17O��HD18O����22��T216O��DT17O��D218O��HT18O����23��T217O��DT18O����24��T218O������Է�������������T218O��
O���͢ݣ�H��D��T���е����ܽ�ϳ�ˮ������ˮ��������������ԭ�Ӻ�һ����ԭ�ӣ�����������ԭ�ӿ����Dz�ͬ����ģ�����ԭ�ӵġ����䡱��6�֣��ʿ��γ�ˮ���ӵ�����Ϊ18��=6��3���֣��ɵ���Է���������ͬ��ˮ��������Ϊ7�֣���Է��������ֱ���18��H216O����19��HD16O��H217O����20��D216O��HT16O��HD17O��H218O����21��DT16O��D217O��HT17O��HD18O����22��T216O��DT17O��D218O��HT18O����23��T217O��DT18O����24��T218O������Է�������������T218O��
��3��![]() H2
H2![]() O��Ħ������Ϊ[(2��2)+16]g��mol-1=20g��mol-1��M(
O��Ħ������Ϊ[(2��2)+16]g��mol-1=20g��mol-1��M(![]() H2
H2![]() O)=22g��mol-1��1��
O)=22g��mol-1��1��![]() H216O���Ӻ�10�����Ӻ�10�����ӣ�1��
H216O���Ӻ�10�����Ӻ�10�����ӣ�1��![]() H218O���Ӻ�10�����Ӻ�12�����ӣ�����
H218O���Ӻ�10�����Ӻ�12�����ӣ�����![]() H216O��
H216O��![]() H218O����1g����1g��
H218O����1g����1g��![]() H216O��1g��
H216O��1g��![]() H218O����������Ϊ(
H218O����������Ϊ(![]() ):(
):(![]() )=11:10����������Ϊ(
)=11:10����������Ϊ(![]() ):(
):(![]() )=11:12��
)=11:12��
��4������![]() H2
H2![]() O��
O��![]() H2
H2![]() O����1g��M(
O����1g��M(![]() H2
H2![]() O)=18g��mol-1��M(
O)=18g��mol-1��M(![]() H2
H2![]() O)=20g��mol-1����n(
O)=20g��mol-1����n(![]() H2
H2![]() O)=
O)=![]() mol��n(
mol��n(![]() H2
H2![]() O)=
O)=![]() mol�������������n(
mol�������������n(![]() H2)=
H2)=![]() mol��n(
mol��n(![]() H2)=
H2)=![]() mol�����ݰ����ӵ����ɿ�֪������������ͬ��ͬѹ�µ����Ϊ
mol�����ݰ����ӵ����ɿ�֪������������ͬ��ͬѹ�µ����Ϊ![]() ��
��![]() =10��9��������Ϊ(
=10��9��������Ϊ(![]() ��2):(
��2):(![]() ��4)=5:9��
��4)=5:9��

����Ŀ����2L�ܱ���������800��ʱ��Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��ϵ����n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ����n(NO)��ʱ��ı仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K��__________��
��2��0��2 s�ڸ÷�Ӧ��ƽ������v(NO)��__________, v(O2)��__________��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����__________��
a��v(NO2)��2v(O2)
b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2)
d���������ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����__________��
a����ʱ�����NO2���塡�� b������O2��Ũ��
c������������� d��ѡ���Ч����