题目内容
下列变化属于吸热反应的是( )
①用镁条引燃铝、氧化铁混合粉末
②碳酸钙受热分解
③浓硫酸稀释
④氢氧化钡晶体和氯化铵固体反应
⑤生石灰和水反应.
①用镁条引燃铝、氧化铁混合粉末
②碳酸钙受热分解
③浓硫酸稀释
④氢氧化钡晶体和氯化铵固体反应
⑤生石灰和水反应.
| A、②④ | B、①④ | C、②③ | D、①⑤ |
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
解答:
解:①铝热反应是放热反应,故①错误;
②碳酸钙受热分解是吸热反应,故②正确;
③强酸强碱溶于水放热,故③错误;
④氢氧化钡晶体和氯化铵固体反应是吸热反应,故④正确;
⑤生石灰和水反应是化合反应是放热反应,故⑤错误.
故选A.
②碳酸钙受热分解是吸热反应,故②正确;
③强酸强碱溶于水放热,故③错误;
④氢氧化钡晶体和氯化铵固体反应是吸热反应,故④正确;
⑤生石灰和水反应是化合反应是放热反应,故⑤错误.
故选A.
点评:本题考查放热反应,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
相关题目
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A、一定有Cl- |
| B、一定有SO42- |
| C、一定没有Al3+ |
| D、一定有CO32- |
下列反应属于放热反应的是( )
A、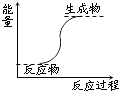 能量变化如图所示的反应 |
| B、燃烧反应和铝热反应 |
| C、化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D、氢氧化钡晶体和氯化铵晶体的反应 |
见光能分解的盐是( )
| A、HClO |
| B、AgBr |
| C、氯水 |
| D、Ca(ClO)2 |
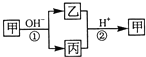 甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )| A、X元素可能为Al |
| B、X 元素不一定为非金属元素 |
| C、反应①和②互为可逆反应 |
| D、反应①和②一定为氧化还原反应 |
构造原理揭示的电子排布能级顺序,实质是各能级能量高低.若以E(nl)表示某能级的能量,以下各式中正确的是( )
| A、E(4s)>E(3s)>E(2s)>E(1s) |
| B、E(4s)>E(3d)>E(3p)>E(3s) |
| C、E(5s)>E(4f)>E(4s)>E(3d) |
| D、E(5s)>E(4s)>E(4f)>E(3d) |
一次实验课后,小明不小心将下列5中液体试剂的标签弄混,他想了一会,不另用任何试剂就能这五种溶液一一鉴别出来,把①CuCl2、②Na2SO4、③KCl、④K2CO3、⑤BaCl2这5种药品鉴别出来的正确鉴别顺序是( )
| A、①②④③⑤ |
| B、④⑤③②① |
| C、①④⑤②③ |
| D、①②④⑤③ |
下列叙述正确的是( )
| A、能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| B、液溴易挥发,在存放液溴的试剂瓶中应加水封存 |
| C、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定存在Ag+ |
 一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )
一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )