题目内容
化学与人们的生活、健康密切相关.下列做法不合理的是( )
| A、用灼烧和闻气味的方法区别棉织物和纯毛织物 |
| B、用透析的手段净化尿毒症患者的血液 |
| C、用米汤检验加碘食盐中的KI03 |
| D、向豆浆中加入盐卤制做豆腐 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:实验评价题
分析:A.纯毛织物的成分为蛋白质;
B.血液为胶体分散系,不能透过半透膜;
C.淀粉遇碘单质变蓝;
D.豆浆为胶体分散系,加盐卤发生聚沉.
B.血液为胶体分散系,不能透过半透膜;
C.淀粉遇碘单质变蓝;
D.豆浆为胶体分散系,加盐卤发生聚沉.
解答:
解:A.纯毛织物的成分为蛋白质,棉织物的成分为纤维,灼烧有烧焦羽毛气味的为纯毛织物,可鉴别,故A正确;
B.血液为胶体分散系,不能透过半透膜,则用透析的手段净化尿毒症患者的血液,故B正确;
C.淀粉遇碘单质变蓝,而加碘食盐中为KI03,不能检验,故C错误;
D.豆浆为胶体分散系,加盐卤发生聚沉,则向豆浆中加入盐卤制做豆腐,故D正确;
故选C.
B.血液为胶体分散系,不能透过半透膜,则用透析的手段净化尿毒症患者的血液,故B正确;
C.淀粉遇碘单质变蓝,而加碘食盐中为KI03,不能检验,故C错误;
D.豆浆为胶体分散系,加盐卤发生聚沉,则向豆浆中加入盐卤制做豆腐,故D正确;
故选C.
点评:本题考查物质的鉴别和检验,为高频考点,把握常见物质的性质及特性为解答的关键,侧重有机物性质、胶体性质、碘的性质及鉴别的考查,题目难度不大.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
下列燃料能实现二氧化碳零排放的是( )
| A、氢气 | B、天然气 |
| C、液化气 | D、沼气 |
下列有关说法正确的是( )
| A、一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B、氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C、升高温度水的离子积常数减小 |
| D、根据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差.
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
Si(s)+4HCl(g),该反应的反应热△H为( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| ||
| A、+412kJ?mol-1 |
| B、-412kJ?mol-1 |
| C、+236kJ?mol-1 |
| D、-236kJ?mol-1 |
“细节决定成败”对于下列实验细节处理正确的是( )
| A、实验室制氢气:为了加快反应速率,向稀H2SO4滴加少量CuSO4溶液 |
| B、钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水 |
| C、配置0.10mol/L NaOH溶液:称取0.4g NaOH放入100mL容量瓶,加水至100mL |
| D、配置FeCl2溶液:称取一定量的FeCl2固体,加水溶解,在加入稀盐酸酸化 |
有①Na2CO3溶液;②CH3COONa溶液、③NaOH溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
| A、三种溶液pH的大小顺序是③>②>① |
| B、若分别加入25mL 0.1mol/L盐酸后,pH最大的是① |
| C、若将三种溶液稀释相同倍数,pH变化最大的是② |
| D、水电离出的氢离子浓度大小顺序是②>①>③ |
下列说法不正确的是( )
A、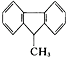 分子中的所有碳原子不可能同时在一个平面内 分子中的所有碳原子不可能同时在一个平面内 |
B、按系统命名法,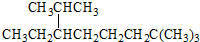 的名称为2,2,7-三甲基-6-乙基辛烷 的名称为2,2,7-三甲基-6-乙基辛烷 |
C、目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET(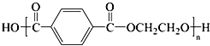 )的合成单体之一是对苯二甲酸 )的合成单体之一是对苯二甲酸 |
| D、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加过量的溴水溶液,观察到溶液褪色,再向溶液中加入新制的Cu(OH)2悬浊液,加热煮沸,观察到砖红色沉淀 |
 短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )
短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )| A、W的单质易溶于CS2 |
| B、Q与R可能形成化合物Q3R4 |
| C、T的最高价氧化物的对应水化物为强碱 |
| D、W、Z都有多种含氧酸 |