题目内容
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
| A.电池放电时,Na+从b极区移向a极区 |
| B.电极a采用MnO2,放电时它被还原 |
| C.该电池负极的电极反应式为BH4-+8OH--8e-=BO2-+6H2O |
| D.放电时,a极区溶液的pH升高,b极区溶液pH降低 |
C
解析

练习册系列答案
相关题目
下列叙述正确的是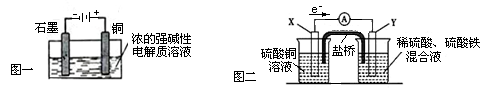
| A.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应 |
| B.图一所示当有0.1mol电子转移时,有0.1molCu2O生成 |
| C.图二装置中发生:Cu+2Fe3+ = Cu2++2Fe2+,X极是负极,Y极材料可以是铜 |
| D.如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中 |
某化学兴趣小组的同学用如图所示装置研究电化学问题。当闭合该装置的电键时,观察到电流计的指针发生偏转。下列有关说法错误的是
| A.甲装置是原电池,乙装置是电解池 |
| B.当甲中产生0.1 mol气体时,乙中析出固体的质量为6.4 g |
| C.实验一段时间后,甲烧杯中溶液的pH增大 |
| D.将乙中的C电极换成铜电极,则乙装置可变成电镀装置 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOClCl)中形成的,其电池总反应方程式为8Li+3SOCl2=6LiCl+Li2SO3+2S。下列叙述中正确的是( )
| A.电解质溶液可以用水,也可以用饱和食盐水 |
| B.电池工作过程中,亚硫酰氯(SOCl2)被还原成Li2SO3 |
| C.电池工作时,锂电极为正极,石墨电极为负极 |
| D.电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1 |
下列说法正确的是 ( )。
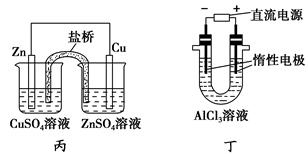
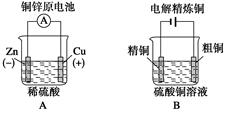
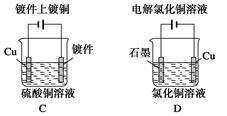
| A.用甲装置电解精炼镁 |
| B.用乙装置验证试管中铁丝发生析氢腐蚀 |
| C.用丙装置构成铜锌原电池 |
| D.用丁装置利用电冶金法制铝 |
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大:
| 金属 | 电子流动方向 | 电压/V |
| 甲 | 甲→Cu | +0.78 |
| 乙 | Cu→乙 | -0.25 |
| 丙 | 丙→Cu | +1.35 |
| 丁 | 丁→Cu | +0.30 |
依据记录数据判断,下列结论中正确的是( )
A.将甲、乙形成的合金露置在空气中,甲先被腐蚀
B.金属乙能从硫酸铜溶液中置换出铜
C.在四种金属中丙的还原性最弱
D.甲、丁若形成原电池时,甲为正极
用Pt作电极,电解含c(Cu2+)∶c(Na+)∶c(Cl-)=1∶2∶4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是( )
A.阴极:2H++2e- H2↑阳极:4OH--4e- H2↑阳极:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
B.阴极:2H++2e- H2↑ 阳极:2Cl--2e- H2↑ 阳极:2Cl--2e- Cl2↑ Cl2↑ |
C.阴极:Cu2++2e- Cu阳极:4OH--4e- Cu阳极:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
D.阴极:Cu2++2e- Cu 阳极:2Cl--2e- Cu 阳极:2Cl--2e- Cl2↑ Cl2↑ |
下图是某同学设计的原电池装置,下列叙述中正确的是( )。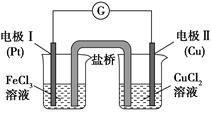
| A.电极Ⅰ上发生还原反应,做原电池的正极 |
| B.电极Ⅱ的电极反应式为Cu2++2e-=Cu |
| C.该原电池的总反应式为2Fe3++Cu=Cu2++2Fe2+ |
| D.盐桥中装有含氯化钾的琼脂,其作用是传递电子 |