��Ŀ����
9��ij�����廯����A�Ľṹ��ʽ�� ��A��һ������������ͼ��ʾ��ת����ϵ��
��A��һ������������ͼ��ʾ��ת����ϵ��
��֪E����ʽΪC9H8O2��
��1��������������ת���У�һ�����漰���ķ�Ӧ������a��
a���ӳɷ�Ӧ b����ȥ��Ӧ c��ȡ����Ӧ d��������Ӧ
��2����E�г������⣬������һ����Ԫ������C��E�Ļ�ѧ����ʽ�ǣ�
 ��д�����з�������Ҫ���E��ͬ���칹��Ľṹ��ʽ��
��д�����з�������Ҫ���E��ͬ���칹��Ľṹ��ʽ�� ��
�� ��
���ٷ����б�����������ȡ�������ұ����ϵ�һ�ȴ���������
��1mol���л���������������Һ��Ӧ�ܲ���4mol Ag
��3����E��ʹ������Ȼ�̼��Һ��ɫ��������NaHCO3��Һ��Ӧ����C��E�Ļ�ѧ����ʽ�ǣ�
 ��
��
���� A�Ľṹ��ʽ��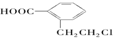 ��������������Һ�����������·���ˮ�ⷴӦ�����ữ�õ�C����BΪ
��������������Һ�����������·���ˮ�ⷴӦ�����ữ�õ�C����BΪ ��CΪ
��CΪ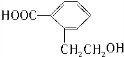 ��C��������������DΪ
��C��������������DΪ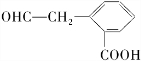 ��C��Ũ���ᡢ���������·�Ӧ�õ�E����E�ķ���ʽΪC9H8O2��Ӧ����ȥ1����ˮ����E��ʹ������Ȼ�̼��Һ��ɫ��������NaHCO3��Һ��Ӧ����F����EΪ
��C��Ũ���ᡢ���������·�Ӧ�õ�E����E�ķ���ʽΪC9H8O2��Ӧ����ȥ1����ˮ����E��ʹ������Ȼ�̼��Һ��ɫ��������NaHCO3��Һ��Ӧ����F����EΪ ��FΪ
��FΪ ����E�г������⣬������һ����Ԫ����Ӧ�Ƿ���������Ӧ����EΪ
����E�г������⣬������һ����Ԫ����Ӧ�Ƿ���������Ӧ����EΪ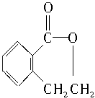 ���Դ˽����⣮
���Դ˽����⣮
��� �⣺��1��������������ת�����漰ȡ����Ӧ��������Ӧ��Cת��ΪE�Ĺ����п��ܷ�����ȥ��Ӧ��һ�����漰�ӳɷ�Ӧ��
�ʴ�Ϊ��a��
��2����E�г������⣬������һ����Ԫ������EΪ ��C��E�Ļ�ѧ����ʽ�ǣ�
��C��E�Ļ�ѧ����ʽ�ǣ� ��
��
��������Ҫ���E��ͬ���칹�壺�ٷ����б�����������ȡ�������ұ����ϵ�һ�ȴ��������֣���1mol���л���������������Һ��Ӧ�ܲ���4mol Ag������������ͬ���칹��Ϊ�� ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
�� ��
��
��3����E��ʹ������Ȼ�̼��Һ��ɫ��������NaHCO3��Һ��Ӧ����F����EΪ ��C��E�Ļ�ѧ����ʽ��
��C��E�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ���ķ����������漰�л���Ӧ���͡��л���Ӧ����ʽ��д����������ͬ���칹����д��ע����ݷ�Ӧ���������ƶϣ��������չ����ŵ�������ת�����ѶȲ���

 ij��ѧС�鹹�뽫����β����NO��NO2��ת��Ϊ��ҪҪ�Ļ���ԭ��HNO3����ԭ����ͼ��ʾ������A��BΪ�������ϣ�����˵��һ����ȷ���ǣ�������
ij��ѧС�鹹�뽫����β����NO��NO2��ת��Ϊ��ҪҪ�Ļ���ԭ��HNO3����ԭ����ͼ��ʾ������A��BΪ�������ϣ�����˵��һ����ȷ���ǣ�������| A�� | �õ�ع���ʱ�����·���ӵ�������A��B���ڵ�·��B��A�γɱպϻ�· | |
| B�� | �缫 B ������ c��H+��Ũ������ | |
| C�� | A �缫�ķ�ӦΪ��NO2-e-+H2O=NO3-+2H+ NO-3e-+2H2O=NO3-+4H+ | |
| D�� | �õ�ع���ʱ��ÿ����11.2LO2������״���£����Գ�ȥ��1molNO��NO2�Ļ��β�� |
| ѡ�� | ʵ��Ŀ�� | ʵ��Ŀ�Ļ���� |
| A | ����̼��Ũ���ᷴӦ���������� | ����������������ͨ����ˮCuSO4������ʯ��ˮ��Ʒ����Һ |
| B | ��ȷ���ס�����Ԫ�طǽ����Ե�ǿ�� | �ⶨͬ��ͬŨ�ȵ�Na3PO4��Na3AsO4ˮ��Һ��pH |
| C | ��ȥCu���л��е�CuO | ����ϡ������Һ�����ˡ�ϴ�ӡ����� |
| D | �Ʊ�Fe��OH��3���� | ��NaOHŨ��Һ�μӵ�����FeCl3��Һ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | C��s��+$\frac{1}{2}$O2��g��=CO��g����H=-396 kJ•mol-1 | |
| B�� | 2H2��g��+O2��g��=2H2O��l����H=-286 kJ•mol-1 | |
| C�� | CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-896 kJ•mol-1 | |
| D�� | CH3OH��l��+O2��g��=CO2��g��+2H2O ��l����H=-736 kJ•mol-1 |
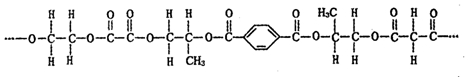
�����й�˵����ȷ���ǣ�������
| A�� | �ø߷�����4�ֵ��壨�ۺϳ��{���ӵļ�С���ӣ����۶��� | |
| B�� | ���ɸ÷��ӵļ��ֿ��ᵥ�廥Ϊͬϵ�� | |
| C�� | ���������е��Ҷ������ɱ�02���������ɵ���֮һ�IJ��� | |
| D�� | �ø߷����й̶��۷е㣬1 mol����������ȫˮ����Ҫ�����������ʵ���Ϊ 5 mol |
| A�� |
| |||||
| B�� |
| |||||
| C�� |
| |||||
| D�� |
|

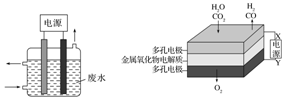 ��ͼ��ʾװ�ó�ȥ��CN-��Cl-��ˮ�е�CN-ʱ��������ҺpHΪ9��10������������ClO-��CN-����Ϊ��������Ⱦ�����壬�����ĵ缫��ӦʽΪ��Cl-+2OH--2e-�TClO-+H2O��
��ͼ��ʾװ�ó�ȥ��CN-��Cl-��ˮ�е�CN-ʱ��������ҺpHΪ9��10������������ClO-��CN-����Ϊ��������Ⱦ�����壬�����ĵ缫��ӦʽΪ��Cl-+2OH--2e-�TClO-+H2O��